

分析 根据图示即可知道仪器名称,根据反应物的状态和反应条件进行分析解答;根据收集氧气的方法进行分析解答;根据一氧化碳还原氧化铁的现象进行解答即可.
解答 解:(1)据图可以看出,仪器②的名称是长颈漏斗,故填:长颈漏斗;
(2)废铁屑与稀盐酸反应制取H2,并控制产生H2的速率,是固体和液体在常温下的反应,可以选用B和D制取,故填:BD;
(3)用排水法收集氧气,氧气应从b端进入,故填:b;
(4)一氧化碳还原氧化铁生成铁和二氧化碳,氧化铁是红色粉末,铁粉是黑色粉末,故会观察到红色粉末逐渐变黑;一氧化碳是有毒的气体,气球能收集尾气中的一氧化碳,防止污染,故填:红色粉末逐渐变黑;收集尾气中的一氧化碳,防止污染.
点评 本题考查的是常见的气体的实验室的制取以及仪器的选择,完成此题,可以依据已有的知识进行.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气中含量最多的元素是氮元素 | |
| B. | 氮气化学性质不活泼,可用于食品防腐 | |
| C. | 空气中的氧气主要来自植物的光合作用 | |
| D. | 空气中的氧气支持燃烧,所以氧气是一种常见的燃料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀有气体原子的最外层电子数(He除外)是8,故最外层电子数为8的粒子一定是稀有气体原子 | |
| B. | 氧化物中含有氧元素,故含有氧元素的化合物一定是氧化物 | |
| C. | 置换反应有单质参加和生成,故置换反应中有元素化合价的改变. | |
| D. | 测定溶液的pH时,若用水将pH试纸湿润,测定结果一定不准确 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
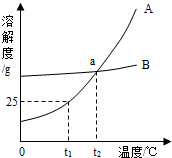 如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | NaOH溶液 | B. | 水 | C. | K2SO4溶液 | D. | Na2CO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
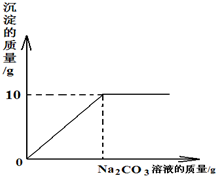 将NaCl 和 CaCl2 的固体混合物21.11克,加入到100克水中,完全溶解后向该混合溶液中逐滴加入质量分数为10%的 Na2CO3 溶液,反应生成 CaCO3 沉淀的质量与所加入的Na2CO3 溶液的质量关系如图所示.回答下列问题:
将NaCl 和 CaCl2 的固体混合物21.11克,加入到100克水中,完全溶解后向该混合溶液中逐滴加入质量分数为10%的 Na2CO3 溶液,反应生成 CaCO3 沉淀的质量与所加入的Na2CO3 溶液的质量关系如图所示.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com