
【题目】某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数。
[查阅资料]
①氢氧化镁和氢氧化铝均难溶于水。难溶性碱受热后能分解生成水和相应的金属氧化物。
②镁和氢氧化镁均不能与氢氧化钠溶液反应,但铝和氢氧化铝分别能与氢氧化钠溶液发生如下反应:![]() ;
;![]() 。
。
氯化铝可与过量氢氧化钠溶液发生反应![]() 。
。
[方案设计]
他们利用实验室提供的盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金![]() 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金![]() 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金![]() 溶液
溶液![]() …→称量灼烧后的固体
…→称量灼烧后的固体
[方案评价]
(1)方案三中最后的灼烧产物的主要成分为水和_____(用化学式表示)。
(2)小段认为三个方案理论上均可行,但方案三不如其它方案,理由是_____。
[实验设计]
实验小组根据方案二设计了如下图所示(图中的铁架台已省略)的实验装置。
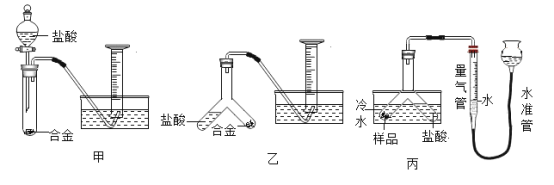
(3)你认为选择装置_____(填“甲”或“乙”)测定镁的质量分数更合理,误差更小,理由是_____。
(4)若装置丙中不使用冷水,则所测得气体的体积会_____(填“偏大”“偏小”或“不变”)。
[交流讨论]
(5)实验小组成员通过交流讨论后重新设计了方案:①称取铝镁合金质量;②加入足量的_____;③过滤;④洗涤;⑤干燥;⑥称取剩余固体的总质量。
【答案】MgO 实验操作相对复杂,使用试剂多 乙 加入的盐酸占装置内体积 偏大 NaOH溶液
【解析】
方案评价:
(1)方案三中。镁铝合金加入盐酸,镁和盐酸反应生成氯化镁和氢气,铝和盐酸反应生成氯化铝和氢气,加入过量氢氧化钠,氯化镁和氢氧化钠生成氢氧化镁沉淀和氯化钠,氯化铝与过量的氢氧化钠反应:![]() ,氢氧化镁、镁不与氢氧化钠反应,故最后灼烧的为氢氧化镁,方案三中最后的灼烧产物的主要成分为水和MgO;
,氢氧化镁、镁不与氢氧化钠反应,故最后灼烧的为氢氧化镁,方案三中最后的灼烧产物的主要成分为水和MgO;
(2)方案三的操作比较复杂,所用试剂较多,故不如其它方案;
实验设计:
(3)装置乙测定镁的质量分数更合理,误差更小,理由是装置甲中加入的盐酸占装置内体积,导致测定的气体体积偏大;
(4)若装置丙中不使用冷水,金属和盐酸反应放热,使气体膨胀,导致所测得气体的体积会偏大;
交流讨论:
(5)实验小组成员通过交流讨论后重新设计了方案:①称取铝镁合金质量;②加入足量的氢氧化钠溶液;③过滤;④洗涤;⑤干燥;⑥称取剩余固体的总质量。因为,铝能与氢氧化钠反应:![]() ,镁不与氢氧化钠反应,故加入足量氢氧化钠溶液,过滤、洗涤、干燥,最后称取剩余镁的质量即可。
,镁不与氢氧化钠反应,故加入足量氢氧化钠溶液,过滤、洗涤、干燥,最后称取剩余镁的质量即可。


科目:初中化学 来源: 题型:
【题目】小山同学在实验室练习初中化学实验硫酸铜与氢氧化钠溶液反应。药品:一定浓度的硫酸铜溶液;质量分数为10%的氢氧化钠溶液小山同学在实验室练习该实验,取100g硫酸铜溶液,逐滴加入氢氧化钠溶液,产生沉淀的质量与加入的氢氧化钠质量的图像如图所示,回答下列问题;
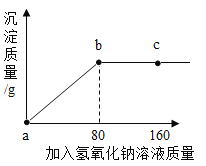
(1)a----b段发生的方程式为__________________。
(2)c点溶液溶质是________________。
(3)求原溶液溶液中硫酸铜的质量分数___________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X.取一定质量的AgNO3固体充分光照,测得反应后生成Ag、O2、X的质量分别为21.6g、mg、9.2g。下列说法正确的是( )
A. AgNO3固体应密封保存在无色细口瓶中
B. m=3.2
C. X的化学式为NO
D. 该反应方程式中Ag与O2的化学计量数之比为3:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图1所示,请回答下列问题:

(1)t2℃时,为配制等质量的甲、乙的饱和溶液,所需水的质量关系是甲____乙(选填“>”、“<”或“=”)。
(2)t℃时,将等质量的甲、乙分别加入到盛有100g水的两个烧杯中,充分溶解后,如图2所示,则下列说法正确的是_________________ 。
A t的取值范围为0≤t≤t1
B 烧杯N所示溶液一定为该温度下乙的不饱和溶液
C 将上述烧杯M中的固体全部溶解后,所得溶液质量一定增大
D 将上述烧杯M中的固体全部溶解后,所得溶液溶质质量分数一定增大或不变
E 若将t升温到t2℃,则M、N两烧杯中溶液的溶质质量分数一定相同
(3)若甲中混有少量乙物质,为提纯甲物质,可供选择的实验步骤如下,正确的操作顺序是______(选填字母)。
A 制取高温下饱和溶液 B 制取低温下饱和溶液 C 降温结晶 D 蒸发结晶 E 过滤
(4)配制室温下100g溶质质量分数一定的乙的溶液,在溶解过程中所需的玻璃仪器是 ______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】比较推理是化学学习中常用的思维方法,下列有关物质的比较推理中正确的是
A.有单质和化合物生成的反应一定是置换反应
B.与酸反应放出气体的物质一定是活泼金属
C.金属元素的原子最外层电子数小于4,所以由金属元素组成的物质中金属元素一定显正价
D.单质中只含有一种元素,所以只含一种元素的纯净物一定是单质
查看答案和解析>>
科目:初中化学 来源: 题型:
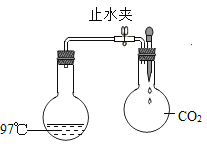
【题目】如图是使水沸腾的实验。先关闭止水夹,将胶头滴管中的液体挤压右侧烧瓶中,然后打开止水夹,发现左侧烧瓶内的水沸腾起来。胶头滴管内的液体可能是_____(填名称),右侧烧瓶中发生反应的化学方程式为_____(合理即可),烧瓶内的水沸腾的原因______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是造福人类的科学。
(1)用适当的化学式填空:
①能供给呼吸的气体________________;
②汽水中含有的酸________________;
③酒精灯内用的燃料________________;
④相对分子质量最小的氧化物________________。
(2)长征五号火箭是现役中国最强运载火箭。请回答下列问题:
①贮箱结构材料选用铝合金,铝合金属于_______________材料 (填“金属”、“合成”或“复合”),铝合金用作火箭材料最主要的优点是________________;
②传统火箭利用偏二甲肼和四氧化二氮作为推进剂,反应的化学方程式为: ___________( 填化学式),四氧化二氮中氮元素的化合价为_____________。
___________( 填化学式),四氧化二氮中氮元素的化合价为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象能正确反映其对应实验操作的是
A. 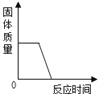 高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石
B.  用等质量、等浓度的双氧水分别制取氧气
用等质量、等浓度的双氧水分别制取氧气
C.  向一定体积的水中逐滴加入氢氧化钠溶液
向一定体积的水中逐滴加入氢氧化钠溶液
D.  某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习小组测定某工业废水(含有H2SO4、HNO3,不含固体杂质)中H2SO4的含量。取100g废水于烧杯中,加入100gBaCl2溶液,恰好完全反应,经过滤得到176.7g溶液。
(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为_______g;
(2)该工业度水中硫酸的质量分数为多少?(写出计算过程)
(3)为避免工业废水污染环境,排放前应对废水进行中和处理,需加入的物质是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com