解:(1)①水在通电的条件下生成氢气和氧气,化学方程式为:2H
2O

2H
2↑+O
2↑,
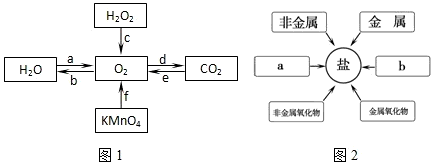
②双氧水分解制氧气时,O
2中会混有的少量杂质水蒸气.
③植物吸收二氧化碳排出氧气的过程叫光合作用
④转化f是高锰酸钾分解制O
2,该反应的反应物是一种,生成物是锰酸钾、二氧化锰和氧气三种,因此基本反应类型是分解反应.
(2)①在溶液中只要有水,水一定作溶剂;
②铁丝燃烧时集气瓶底部放少量的水是防止生成物溅落瓶底,使集气瓶炸裂;
③由于进入水体积正好是集气瓶容积的

所以可得出氧气约占空气总体积

的结论;
④热水温度达到了白磷的着火点,能使铜片上的白磷燃烧,所以提供了热量,使水中白磷不能燃烧,是验证没有氧气是否能燃烧,所以水的作用是隔绝空气;
⑤二氧化碳与水反应生成碳酸,所以水是反应物,二氧化碳能溶于水,因此水还作溶剂
(3)酸和碱都能与某些物质反应生成盐,所以本题答案为:酸,碱;
(4)根据图示可以看出,要生成硫酸亚铁,可以使用金属铁或铁的氧化物与稀硫酸的反应,铁能与稀硫酸反应生成硫酸亚铁和氢气,氧化亚铁能与硫酸反应生成硫酸亚铁和水,化学方程式为:Fe+H
2SO
4═FeSO
4+H
2↑,FeO+H
2SO
4═FeSO
4+H
2O.
故答案为:(1)①①2H
2O

2H
2↑+O
2↑.
②水蒸气.③光合.④分解反应
(2)①溶剂;②炸裂;③

④隔绝空气;⑤溶剂和反应物.
(3)酸,碱.
(4)Fe+H
2SO
4=FeSO
4+H
2↑; H
2SO
4+FeO=FeSO
4+H
2O.
分析:(1)①根据电解水会生成氢气和氧气进行分析,
②根据双氧水分解制氧气的实际过程进行分析,
③根据植物吸收二氧化碳转化为氧气的原理进行分析,
④根据实验室制氧的原理进行分析.
(2)①根据溶剂的判断方法考虑;②根据铁丝燃烧实验分析③根据氧气的含量考虑;④根据热水的作用考虑;⑤根据二氧化碳能溶于水,能与水反应考虑.
(3)酸和碱都能反应生成盐
(4)铁能与酸反应生成亚铁盐,铁的氧化物氧化亚铁能与酸反应生成亚铁盐.
点评:在解方程式的书写题时,首先判断反应原理,然后根据方程式的书写规则进行书写.了解水的性质和常见的一些用途,记住常见盐的化学性质以及有关反应化学方程式的书写,完成此题,可以依据已有的知识进行,要求同学们加强对物质间反应的识记,以便灵活应用.


 2H2↑+O2↑,
2H2↑+O2↑, 所以可得出氧气约占空气总体积
所以可得出氧气约占空气总体积 的结论;
的结论; 2H2↑+O2↑.
2H2↑+O2↑. ④隔绝空气;⑤溶剂和反应物.
④隔绝空气;⑤溶剂和反应物.

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案