
| ||


 小学课时特训系列答案
小学课时特训系列答案科目:初中化学 来源: 题型:
| A、将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水就是纯水 |
| B、用肥皂水不可以区分硬水和软水 |
| C、洗涤剂能洗涤餐具上油污的原因是洗涤剂可以使油脂乳化 |
| D、稀释浓硫酸时,将水倒入浓硫酸中,并不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
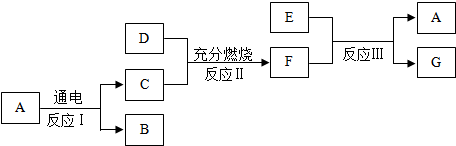
查看答案和解析>>
科目:初中化学 来源: 题型:
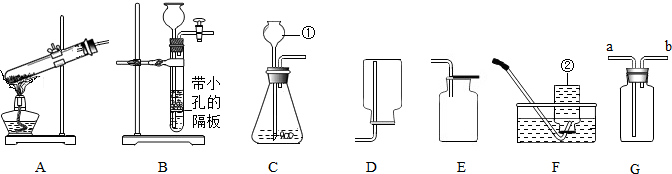
查看答案和解析>>
科目:初中化学 来源: 题型:
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
| 稀盐酸的质量/g | 15 | 30 | 45 | 60 |
| 生成气体的质量/g | 1.8 | n | 4.4 | 4.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
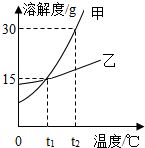 如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com