
【题目】水是生命之源。
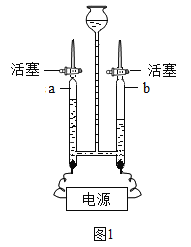
(1)用如图1所示装置进行电解水的实验,该反应的化学方程式为_____。一段时间后a、b两玻璃管中收集到的气体体积比约为_____。
(2)生活中可用_____区分硬水和软水;家庭中常用_____方法将硬水转化为软水,该方法会使家中水壶中产生水垢,家庭中可用_____(填一种调味品名称)除去水壶内壁上的水垢。
(3)如图2是自来水厂净化水的主要步骤。
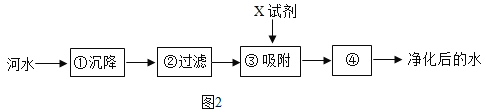
有关说法正确的是_____(填字母编号)
A 步骤①中可加入明矾作絮凝剂
B X试剂可以是活性炭
C 步骤④的作用是消毒杀菌
D 净化后的水为纯净物
【答案】2H2O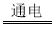 2H2↑+O2↑ 1:2 肥皂水 加热煮沸(或煮沸,只写加热不给分) 食醋 ABC
2H2↑+O2↑ 1:2 肥皂水 加热煮沸(或煮沸,只写加热不给分) 食醋 ABC
【解析】
(1)电解水的产生氢气和氧气的化学方程式为2H2O![]() 2H2↑+O2↑。一段时间后a管产生气体少是氧气、b管产生气体多是氢气,两玻璃管中收集到的气体体积比约为1:2。
2H2↑+O2↑。一段时间后a管产生气体少是氧气、b管产生气体多是氢气,两玻璃管中收集到的气体体积比约为1:2。
(2)生活中可用肥皂水区分硬水和软水,将其分别混合后搅拌,浮渣多、泡沫少的是硬水,反之是软水;家庭中常用加热、煮沸的方法将硬水转化为软水,该方法会使家中水壶中产生水垢,家庭中可用食醋(主要含有醋酸)除去水壶内壁上的水垢。因为醋酸显酸性能和水垢(碳酸钙)发生反应,达到除垢效果;
(3)有关说法正确的是:
A、步骤①中可加入明矾作絮凝剂,可以吸附悬浮杂质;故选项正确;
B、X试剂可以是活性炭,具有吸附性,能吸附色素和异味;故选项正确;
C、步骤④的作用是消毒杀菌,达到饮用水标准;故选项正确;
D、净化后的水中依然还有可溶性物质,属于混合物;故选项错误;
故选:ABC。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如图所示。根据图中信息回答下列问题:
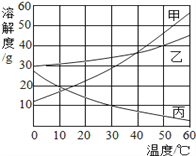
(1)50℃时,乙物质的溶解度是______,该温度下其饱和溶液溶质的质量分数为______(结果精确到0.1%);
(2)50℃时,将甲、乙、丙三物质的饱和溶液各500g分别蒸发掉100g水,析出晶体的质量由小到大的顺序是_______________;
(3)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是______。
(4)要配制110g溶质质量分数为9.1%的丙物质溶液,配制时溶液的温度需要控制的范围是___________℃。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组对“测定空气中氧气的含量”的实验进行改进,如图II,收到了良好的效果。已知,试管 体积为90mL,实验前,关闭弹簧夹,注射器活塞停在30ml处,实验后打开弹簧夹。下列说法正确的是( )
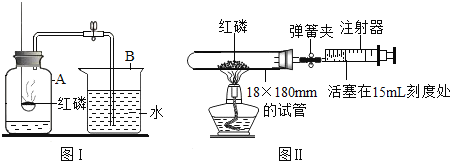
a.图I实验中,进入集气瓶中水的体积不到瓶中空气体积的1/5,可能是由于点燃红磷后.塞回到集气瓶时瓶塞没有塞紧
b.图II实验结束后打开弹簧夹,注射器活塞应停在12mL刻度处
c.图II实验中若弹簧夹始终打开,实验结束后注射器活塞最终仍应停留在12mL刻度处
d.图II与图I的实验相比,不仅实验结果更加准确,而且减少了空气污染
e.若图II中弹簧夹始终打开进行实验,可以看到注射器活塞开始时静止,最终向左移动
A.abdB.abcC.abeD.acd
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】比较与归纳是我们学习化学的常用方法。请结合下图中实验常用装置,回答有关问题。
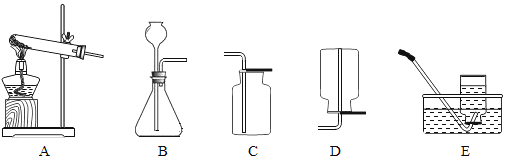
(1)若用B、E组合装置制取氧气,发生反应的化学方程式为_____。
(2)实验室通常用稀盐酸和石灰石反应制取CO2,应选用的发生装置和收集装置分别为_____和_____(填序号,下同),选用此发生装置的条件是_____。
(3)CO2也可以用碳酸氢钠(NaHCO3)固体加热分解[产物为碳酸钠(Na2CO3)、二氧化碳和水]来制取,该反应的化学方程式为_____,若用此法来制取CO2,应选用的发生装置是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂车间以MnO2为原料制备高纯MnCO3的流程如下。下列说法正确的是( )
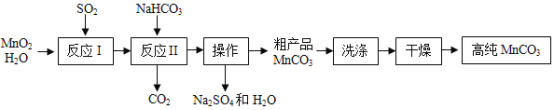
已知:①反应I的化学方程式:MnO2+SO2=MnSO4;
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100°C时开始分解。
A.反应I中只有Mn元素的化合价发生了改变
B.反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有Mn(OH)2
C.为快速获得高纯MnCO3,需选择干燥的条件是高于100°C
D.若原料MnO2有8.7kg,假设其它原料都足量,实验过程无损失,最终得到的产品中含11.5kgMnCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图一所示,三个充满CO2气体的烧瓶,注射器内各装有85mL的液体(分别是水、饱和石灰水、40%的氢氧化钠溶液)。同时将注射器内液体注入烧瓶中,关闭活塞。观察到烧瓶内气压变化图像如图二所示。
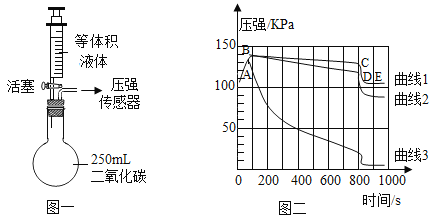
(1)曲线2发生反应的化学方程式为_________________________________。
(2)通过上述三条曲线的对比可得出除去CO2气体应选择的试剂是__________________。
(3)请设计实验证明曲线3反应后溶液中可能所含的溶质,简要写出步骤和现象)_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气、水是我们赖以生存的重要资源。
(1)氧气约占空气体积的___________。
(2)实验室中常用红磷燃烧来测量空气中氢气的体积含量,反应的化学方程式为: _________。
(3)从长江里取出的“水”属于_________(填纯净物或混合物).
(4)“节约用水,人人有责”,下列生活中节水措施错误的是_______(填标号).
A 洗脸刷牙,随手关水
B 洗菜用水,用来浇花
C 少喝水以节约用水
D 水管漏水,及时修理
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现用质量分数为29.2%的盐酸溶液配制500g质量分数为7.3%的稀盐酸,用所配稀盐酸测得某NaOH溶液的溶质质量分数为20%。
(1)需要加入_____g水来配得上述稀盐酸。
(2)测得溶液pH=7时,消耗稀盐酸200g。求恰好完全反应时,所得溶液中溶质质量分数。_____(写出计算过程,计算结果保留一位小数)
(3)若所测NaOH溶液在空气中放置时间较长,已经变质,那么测定的NaOH质量_____(填“偏大”、“偏小”、“不变”或“无法确定”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】 化学反应前后各物质的质量总和是否相等?
【查阅资料】 氢氧化钠溶液可以吸收二氧化碳气体
【猜想与假设】 猜想1:不相等;猜想2:相等。
【实验探究】 甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | _________,天平指针没有偏转 |
结论 | 猜想1正确,反应的化学方程 式:_______________. | 猜想2正确 |
【反思评价】 究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_______________中进行。
【优化装置】 同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号)___,从另外两种装置中任选一种指出其不足:________。
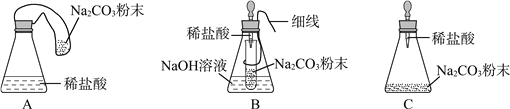
【得出结论】 同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步
分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_________________________的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】
解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_________种元素组成。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com