
【题目】下列叙述体现了质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
D.100g 质量分数为30%的过氧化氢溶液中,含有30g过氧化氢和70g水
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】硫酸铁铵[NH4Fe(SO4)2]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图。请根据流程图回答下列问题。
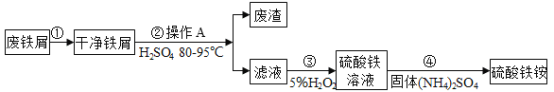
(1)步骤③的化学方程式为![]() ,在这个化学变化过程中,化合价发生改变的元素为:_____。
,在这个化学变化过程中,化合价发生改变的元素为:_____。
(2)步骤④发生化合反应,写出该反应的化学方程式_____。
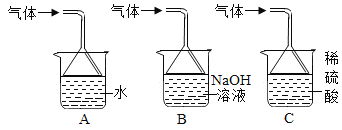
(3)步骤①会产生有毒的SO2,图中最适合吸收SO2防止造成空气污染的装置是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小立在家洗衣服时,发现一瓶刚过期的漂白液,于是对该漂白液的漂白原理、是否还有效及其成分是什么等问题产生了兴趣,于是将其带到学校,在老师的指导下,与小组同学一起展开探究。
(查阅资料)
①制取漂白粉的原理:Cl2+2NaOH═NaClO+NaCl+H2O,其中有效成分是NaClO;
②漂白液的漂白原理:
NaClO在空气中很快发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO
生成的HClO能使有色物质褪色;
③HClO不稳定,受光照时易分解生成HCl和一种常见气体。
(进行实验)小组同学通过实验,证明了该漂白液已完全失效,他们的实验方法及观察到的现象是__________________________________________________。
(交流讨论)该小组同学经过分析得出:HClO分解除生成HCl外,生成的另外一种常见气体是_______(写化学式),验证该气体的方法是______________________________。
(提出问题)该漂白液的成分是什么?
(作出猜想)猜想一:NaCl
猜想二:NaCl、Na2CO3
猜想三:NaCl、Na2CO3、NaOH
(进行实验)
(1)小立验证猜想三。他向该漂白液中滴加酚酞溶液,观察到溶液变红,证明猜想三正确。大家一致认为小立的实验方案不科学,原因是__________________。
(2)小刚取适量该漂白液于试管中,滴加足量稀盐酸,观察到有大量气泡产生,证明溶液中一定含有Na2CO3,从而否定了猜想一。Na2CO3与稀盐酸反应的化学方程式为_____________________________________。
(3)为了进一步验证是否含有NaOH,大家经过讨论最终达成了一致意见:向该漂白液中滴加CaCl2溶液至不再产生沉淀为止,加入_________,无明显现象,证明猜想三不正确,从而证明猜想二正确。该实验中若用饱和石灰水代替CaCl2溶液是否可行?____________为什么?__________________________________。
(反思拓展)
(1)为了避免漂白液失效,我们在保存和使用时应避免光照,用完后及时拧紧瓶盖。
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工业废料含碱式碳酸铜(Cu2(OH)2CO3)和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下。
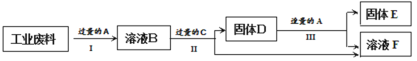
已知:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ Fe+Fe2(SO4)3=3FeSO4
(1)进行过滤操作的是过程______(填“Ⅰ”“Ⅱ”“Ⅲ”)。
(2)过程Ⅲ加入适量A的化学方程式是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从A~C中任选两个作答,若均作答,按前两个计分。
序号 | A | B | C |
实验 装置 |
|
|
|
问题 | 该实验的目的是_____。 | 若用此实验成功验证质量守恒定律,改进的方法是_____。 | 能说明铜具有导热性的现象是_____。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液在生产、生活中十分常见。
(1)水常用于灭火,其灭火原理是_______。
(2)自来水厂净水过程的主要操作流程如下图:
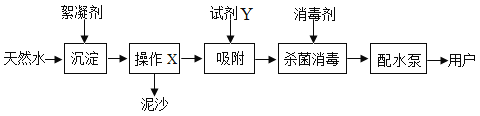
资料:常用的絮凝剂有明矾,消毒剂有液氯(Cl2)。
回答下列问题:
①操作X的名称是______,试剂Y的名称是______。
②明矾作絮凝剂是因为明矾溶于水后生成的__对杂质的吸附,使杂质沉降来达到净水的目的。
③Cl2与水反应生成盐酸和次氯酸(HClO),次氯酸有氧化杀毒作用。写出Cl2与水反应的化学方程式_____,HClO中Cl的化合价为_______价。
④自来水厂的净水过程______(填“能”或“不能”)将硬水软化成软水,生活中将硬水软化的常用方法是_____。
⑤甲、乙两种固体的溶解度曲线如下图所示。下列说法中,正确的是______。
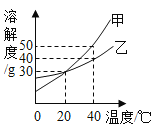
A 20°C时,相同质量的甲、乙溶液,溶质的质量分数一定相等
B 40°C时,将相同质量的甲、乙分别配制成饱和溶液,甲需要水的质量比乙少
C 40°C时,分别在100g水中加入40g甲、乙,同时降温至20°C,过滤,得到甲、乙两种固体的质量一样多
D 20°C时,分别在100g水中加入50g甲、乙,加热到40°C时,甲、乙固体全部消失,均形成饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像与对应的说法正确的是
A.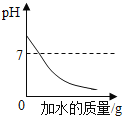 向NaOH溶液中加水稀释
向NaOH溶液中加水稀释
B.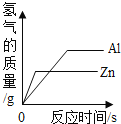 等质量的Al、Zn与足量的稀硫酸反应
等质量的Al、Zn与足量的稀硫酸反应
C.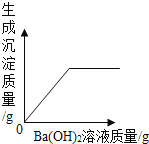 向稀硫酸中加入Ba(OH)2溶液
向稀硫酸中加入Ba(OH)2溶液
D.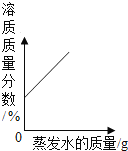 在恒温的条件下,适量蒸发饱和NaCl溶液的水分
在恒温的条件下,适量蒸发饱和NaCl溶液的水分
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化钠是实验室常用的一种试剂。
(1)向盛有2mL稀氢氧化钠溶液的试管中,滴入几滴无色酚酞溶液,可以观察到溶液变成红色,使酚酞溶液变红的粒子是_____(填化学符号)。
(2)向盛有2mL稀氢氧化钠溶液的试管滴加硫酸铜溶液,现象是_____,发生反应的化学方程式是_____。
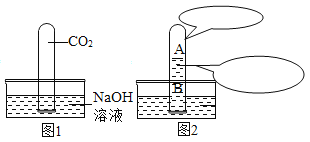
(3)下图为CO2与足量NaOH溶液反应示意图。图1为松开橡皮塞前的状态,图2为松开橡皮塞一段时间后的状态。请画出图2试管中A区和B区的主要微观粒子组成示意图,并进行必要的标注_____(水分子不用画出)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com