
【题目】小立在家洗衣服时,发现一瓶刚过期的漂白液,于是对该漂白液的漂白原理、是否还有效及其成分是什么等问题产生了兴趣,于是将其带到学校,在老师的指导下,与小组同学一起展开探究。
(查阅资料)
①制取漂白粉的原理:Cl2+2NaOH═NaClO+NaCl+H2O,其中有效成分是NaClO;
②漂白液的漂白原理:
NaClO在空气中很快发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO
生成的HClO能使有色物质褪色;
③HClO不稳定,受光照时易分解生成HCl和一种常见气体。
(进行实验)小组同学通过实验,证明了该漂白液已完全失效,他们的实验方法及观察到的现象是__________________________________________________。
(交流讨论)该小组同学经过分析得出:HClO分解除生成HCl外,生成的另外一种常见气体是_______(写化学式),验证该气体的方法是______________________________。
(提出问题)该漂白液的成分是什么?
(作出猜想)猜想一:NaCl
猜想二:NaCl、Na2CO3
猜想三:NaCl、Na2CO3、NaOH
(进行实验)
(1)小立验证猜想三。他向该漂白液中滴加酚酞溶液,观察到溶液变红,证明猜想三正确。大家一致认为小立的实验方案不科学,原因是__________________。
(2)小刚取适量该漂白液于试管中,滴加足量稀盐酸,观察到有大量气泡产生,证明溶液中一定含有Na2CO3,从而否定了猜想一。Na2CO3与稀盐酸反应的化学方程式为_____________________________________。
(3)为了进一步验证是否含有NaOH,大家经过讨论最终达成了一致意见:向该漂白液中滴加CaCl2溶液至不再产生沉淀为止,加入_________,无明显现象,证明猜想三不正确,从而证明猜想二正确。该实验中若用饱和石灰水代替CaCl2溶液是否可行?____________为什么?__________________________________。
(反思拓展)
(1)为了避免漂白液失效,我们在保存和使用时应避免光照,用完后及时拧紧瓶盖。
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题。
【答案】取适量漂白液于烧杯中,放入有色的布条,发现布条没有明显变化 O2 用集气瓶收集产生的气体,放入带火星的木条,观察是否复燃 若溶液中有Na2CO3,也能使无色酚酞变红 ![]() 酚酞溶液 不可行 氢氧化钙与碳酸钠反应生成氢氧化钠,会干扰检验
酚酞溶液 不可行 氢氧化钙与碳酸钠反应生成氢氧化钠,会干扰检验
【解析】
进行实验:
根据题目信息可知,NaClO可溶于水,漂白原理是:它在空气中发生反应![]() ,HClO能使有色物质如有色布条,所以若观察到有色布条不褪色则说明该漂白液已完全失效;故实验方法及观察到的现象是:取适量漂白液于烧杯中,放入有色的布条,发现布条没有明显变化。
,HClO能使有色物质如有色布条,所以若观察到有色布条不褪色则说明该漂白液已完全失效;故实验方法及观察到的现象是:取适量漂白液于烧杯中,放入有色的布条,发现布条没有明显变化。
交流讨论:
HClO分解除生成HCl外,根据质量守恒定律可知,生成的另外一种常见气体是氧气,化学式为O2,验证氧气的方法是:用集气瓶收集产生的气体,放入带火星的木条,观察是否复燃。
进行实验:
(1)“向该漂白液中滴加酚酞溶液,观察到溶液变红,证明猜想三正确”,实验方案不科学,原因是:若溶液中有Na2CO3,也能使无色酚酞变红。
(2)Na2CO3与稀盐酸反应生成氯化钠、二氧化碳和水,反应的化学方程式为 ![]() 。
。
(3)为了进一步验证是否含有NaOH,可向该漂白液中滴加氯化钙溶液至不再产生沉淀为止,除去碳酸钠,加入酚酞溶液,无明显现象,证明猜想三不正确,从而证明猜想二正确。该实验中若用饱和石灰水代替氯化钙溶液是不可行的,因为氢氧化钙与碳酸钠反应生成氢氧化钠,会干扰检验。


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:初中化学 来源: 题型:
【题目】请根据下列实验装置回答问题:
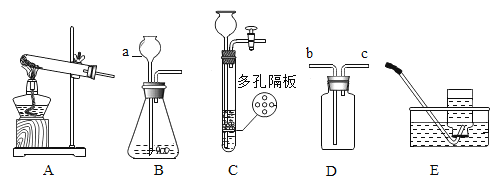
(1)写出图中标有字母a的仪器名称___________________。
(2)用高锰酸钾制取氧气的化学方程式为_____________________,用E装置收集O2,如何判断O2已经收集满______________。
(3)氨气(NH3)是一种无色有刺激性气味,密度比空气小,极易溶于水的气体。实验室常用氯化铵固体和氢氧化钙粉末混合加热来制取氨气。应选用的发生装置是________,如果用D装置收集该气体,则气体从_______端进入(填“b”或“c”)。
(4)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入__________(填写试剂名称)。该反应的化学方程式是_____________________。实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是________________。
(5)如下表所示,除去CO中少量的CO2,选用的试剂和装置都正确的是_____。
选项 | A | B | C |
试剂 | NaOH溶液 | CuO固体 | 浓硫酸 |
部分 装置 |
|
|
|
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:(已知氢氧化铝能溶解在氢氧化钠溶液中,生成偏铝酸钠NaAlO2)
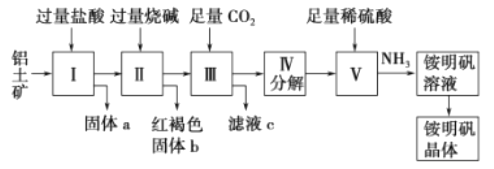
请回答下列问题:
(1)固体a的化学式为_____,Ⅲ中通入足量CO2气体能生成氢氧化铝和一种酸式盐。写出发生反应的化学方程式为_____。
(2)IV步分解指加热使氢氧化铝分解为相应的氧化物。由V制取铵明矾溶液的化学方程式为_____,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_____、冷却结晶、过滤洗涤。
(3)以1000kg含氧化铝30.6%的铝土矿为原料制取Al2(SO4)3,需消耗含溶质质量为_____g的98%的浓硫酸(密度1.84g·cm-1)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的“微粒”个数之比为1:1,则投料时铝土矿中的AI2O3和H2SO4的“微粒”个数之比为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学常见的物质。A是胃酸的主要成分,D是一种钠盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产,C、E为氧化物,C是参与光合作用的气体。它们间的相互关系如图所示(“—”表示两种物质能发生化学反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。请回答:
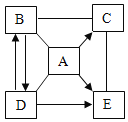
(1)A的化学式_____;C的化学式_____。
(2)A与D反应的化学方程式_____。
(3)B→D反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】央视《是真的吗?》节目中,主持人做了“电池+口香糖铝箔纸=取火工具”的实验,如图所示:

铝箔纸是在纸的表面涂上一层铝箔。取铝箔纸,将其剪成中间窄两头宽的条状,将带铝箔一面的两端分别接在电池的正极和负极,很快发现纸条中间较窄处开始冒烟,起火苗。请同学们据此回答下列问题:
(1)该实验说明铝具有______________性。(写出铝的一条物理性质)
(2)铝箔纸起火的原因是________________________________________。
(3)写出铝箔燃烧的化学方程式________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在物质的宏观、微观和符号之间建立联系是化学学科的特点。请结合图示回答下列问题:
(1)物质的组成和构成如图所示,图中①表示的是___________。
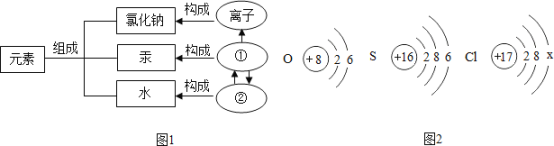
(2)图 2 是氧、硫、氯三种元素的原子结构示意图。
① 氯原子的结构示意图中 x 的数值是___________。
② 氧和硫两种元素的化学性质具有相似性的原因是它们原子的___________相同。
③ 硫的最高价氧化物的水化物为硫酸,将等质量等溶质质量分数的氢氧化钠溶液与稀硫酸充分混合,所得溶液与下列物质不反应的是 ___________(填字母)。
A CuSO4B Fe C BaCl2D SO2
④稀盐酸、稀硫酸具有相似的化学性质,是因为溶液中都含有相同的____________(填离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】磷酸二氢铵(NH4H2PO4)是一种化肥,它对提高农作物的产量具有重要作用。按要求计算:
(1)NH4H2PO4中氮、氢、氧原子的个数比为 ;
(2)NH4H2PO4的相对分子质量是 ;
(3)NH4H2PO4中氮元素和氢元素的质量比为 (写最简比);
(4)11.5 g NH4H2PO4中含磷元素的质量为 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述体现了质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
D.100g 质量分数为30%的过氧化氢溶液中,含有30g过氧化氢和70g水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生产、生活息息相关,请运用化学知识回答下列问题:
(1)下列物质属于合成材料的是_____________(填字母)
A 聚乙烯B 棉花C 合成橡胶D 桑蚕丝
(2)有些村庄需打深井取用地下水,可用_____________区分地下水是软水还是硬水,生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是______________。
(3)提倡少用煤、______________、天然气三大化石燃料,有利于改善空气质量。
(4)新冠肺炎疫情期间,84消毒液是常见的消毒剂。
①84消毒液和洁厕灵混合使用时会发生化学反应2 HCl+NaClO= NaCl+H2O+X,X气体有毒,因此二者不能混合使用。那么X的化学式为________。
②教室喷洒过消毒液后,室内充满消毒液气味,说明分子具有的特性为_________。
(5)熟石灰在生产生活中用途广泛,既可以与________(填化学式)按一定比例符合制备波尔多液,又可以用来改良_____________(填“酸性”、“中性”或“碱性”)土壤。
(6)铁是年产量最高的金属材料。某钢铁厂每天需消耗3500t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是__________t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com