
分析 (1)根据反应物和生成物写出有关反应的化学方程式;铵态氮肥不能与碱性物质混合施用;
(2)根据反应物的状态和反应的条件以及氨气的密度来分析;
(3)根据反应的原理来书写化学方程式以及判断反应的类型,根据氨气有刺激性气味的气体,极易溶于水分析逃生的措施;
(4)根据C装置制取气体的过程考虑优点.
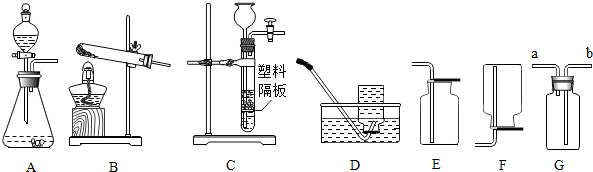
解答 解:(1)氯化铵能与氢氧化钠工业生成氯化钠、水和氨气,由于铵态氮肥与碱性物质混合施用会生成氨气,导致肥效降低,故铵态氮肥不能与碱性物质混合施用;故填:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;碱;
(2)实验室中用固体加热来制取氨气,故选择装置B;氨气的密度比空气小,所以氨气从短管进入,故填:B;a;
(3)氨气与氧气在点燃的条件下反应生成水和氮气,属于一种单质与一种化合物反应生成新的单质与新的化合物,属于置换反应;由于氨气有刺激性气味的气体,极易溶于水,所以,在遇到氨气泄漏时,应该采取的自救措施是用湿毛巾(或衣物)捂住口鼻,立即逆风逃生.故填:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;置换反应;用湿毛巾(或衣物)捂住口鼻,立即逆风逃生;
(4)C装置中的有空塑料板上放锌粒,反应发生时打开开关,硫酸从长颈漏斗内流下,与锌粒接触反应开始,当关闭开关时气体无法排出,压强越来大,把硫酸又压回到长颈漏斗内,使锌粒与硫酸分离,所以反应停止,所以该装置可以控制反应的发生和停止;故填:能控制反应的发生和停止.
点评 正确解读题目给出的信息是解决信息性题目的关键,要善于从信息中捕捉最有效的信息用来处理问题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用熟石灰改良酸性土壤 | |
| B. | 用生石灰做干燥剂 | |
| C. | 用小苏打中和面团发酵中产生的有机酸 | |
| D. | 活性炭使红墨水褪色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 试管号 | 1%淀粉溶液 | 1%稀硫酸 | 蒸馏水 | 碘液 |
| 1 | 2mL | 0 | 1mL | 2滴 |
| 2 | 2mL | 1mL | 0 | 2滴 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | d1>d2 | B. | d1<d2 | C. | d1=d2 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com