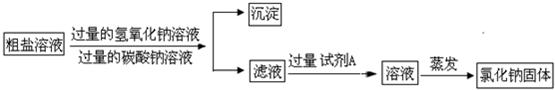
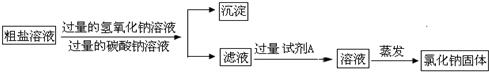
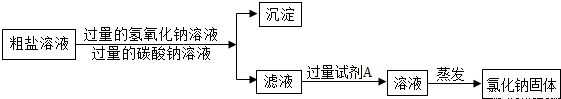
实验室有一包含有少量MgCl2和CaCl2的粗盐,某小组同学要得到纯净的氯化钠固体,进行了如下实验.请回答相关问题:
第一步:除去氯化镁,将粗盐加水溶解,向其中加入过量的氢氧化钠溶液并搅拌,产生白色沉淀,过滤.发生反应的化学方程式为________.
某同学提出:“如果把氢氧化钠溶液换成氢氧化钾溶液,行不行?”小组同学经讨论,一致认为不可行.理由是________.
第二步 除去氯化钙,向滤液中加入过量的________溶液并搅拌,产生白色沉淀,过滤.
第三步 得到氯化钠固体,向第二步实验后的滤液中加入过量的稀盐酸并搅拌,加热蒸发,得到氯化钠固体.加入过量稀盐酸的目的是________.
MgCl2+2NaOH═2NaCl+Mg(OH)2↓ 会有氯化钾新杂质生成 碳酸钠 用稀盐酸除去过量的氢氧化钠和碳酸钠溶液或把过量的氢氧根离子和碳酸根离子
分析:这是一道分离提纯的综合实验题,除杂的基本原则是除掉原杂质又不引入新的杂质,物理方法首选,化学方法次之,解题时重点考虑各种复分解反应的产物.
解答:(1)加入氢氧化钠过量是除掉杂质氯化镁,生成物为氢氧化镁沉淀与氯化钠;如果把氢氧化钠溶液换成氢氧化钾溶液,产物中会有新杂质氯化钾出现.故答案为:MgCl2+2NaOH═2NaCl+Mg(OH)2↓;会有氯化钾新杂质生成;
(2)碳酸钠溶液与氯化钙反应(Na2CO3+CaCl2═CaCO3↓+2NaCl),从而除掉氯化钙;
(3)分析整个除杂过程:在反应中氢氧化钠碳酸钠加入量都是过量的,因此要加入过量的盐酸除掉使其转化为氯化钠.用稀盐酸除去过量的氢氧化钠和碳酸钠溶液或把过量的氢氧根离子和碳酸根离子等.
故答案为:第一步:MgCl2+2NaOH═2NaCl+Mg(OH)2↓;会有氯化钾新杂质生成;
第二步 碳酸钠;第三步 用稀盐酸除去过量的氢氧化钠和碳酸钠溶液或把过量的氢氧根离子和碳酸根离子
点评:分离混合物的原则是:①首先考虑物理方法,物理方法不可行再考虑化学方法.
②用化学方法分离杂质时应不能带入或生成新的杂质.