(2012?乐陵市一模)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用.
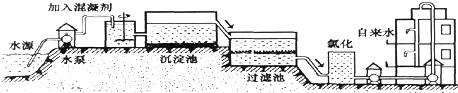
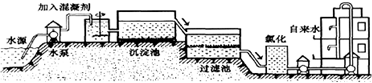
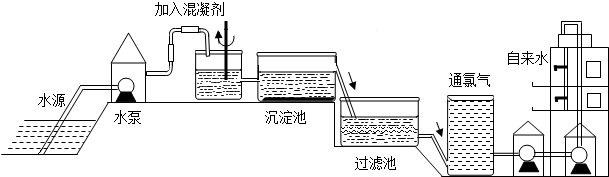
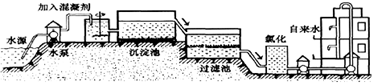
(1)自来水的生产过程大体如下图:

如图过滤池中有活性炭,活性炭起
吸附
吸附
作用,该过程发生的
物理
物理
变化.氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸,其反应化学方程式为
Cl2+H2O=HCl+HClO
Cl2+H2O=HCl+HClO
.实验室配置AgNO
3溶液时不宜用自来水,其原因是(用化学方程式表示)
AgNO3+HCl=AgCl↓+HNO3
AgNO3+HCl=AgCl↓+HNO3
.高铁酸钾(K
2FeO
4)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是
+6
+6
.
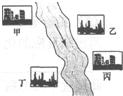
(2)如图,在河旁有甲、乙、丙、丁四座工厂,每个工厂排出的废液只含有Na
2CO
3、FeCl
3、NaOH、HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水中有红褐色物质生成;丙处河水由浑变清;丁处产生气泡,河水澄清.请回答:

①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是
无色酚酞或紫色石蕊试液
无色酚酞或紫色石蕊试液
.
②乙处河水有红褐色物质生成的化学方程式是
3NaOH+FeCl3═Fe(OH)3↓+3NaCl
3NaOH+FeCl3═Fe(OH)3↓+3NaCl
.
③丁处产生气泡的化学方程式是
Na2CO3+2HCl═2NaCl+CO2↑+H2O
Na2CO3+2HCl═2NaCl+CO2↑+H2O
.
(3)保护水资源,我们应该采取的措施是
工农业生产中减少甚至消除水体污染物的产生或农业生产中使用高效低毒的农药、化肥
工农业生产中减少甚至消除水体污染物的产生或农业生产中使用高效低毒的农药、化肥
.



 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案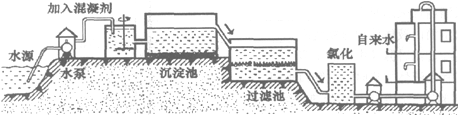
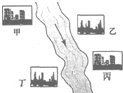 HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清.请回答:
HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清.请回答: