
 某微粒的结构示意图如图所示,下列有关该微粒的说法不正确的是( )
某微粒的结构示意图如图所示,下列有关该微粒的说法不正确的是( )| A. | 原子核内有17个质子 | B. | 原子核外有3个电子层 | ||
| C. | 是一种阳离子 | D. | 在化学反应中可以失去1个电子 |
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 无锈铁钉置于稀硫酸中,表面产生气泡,溶液由无色逐渐变成黄色 | |
| C. | 在潮湿的空气中,铁钉表面逐渐产生疏松的红棕色固体 | |
| D. | 铁钉浸没在硫酸铜溶液中,表面覆盖了一层红色物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去KCl溶液中混有的 K2 SO4 | 加入过量的BaCl2溶液 |
| B | 鉴别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液 | 不用其它任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③② |
| C | 使Fe(OH)3一步转化为 FeCl3 | 唯一的方法只能加入稀盐酸 |
| D | 鉴别NaCl溶液、NaOH溶液和 BaCl2溶液 | 各取少量于试管中,分别滴加 CuSO4溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
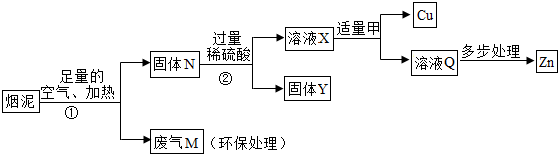
| A. | ②、③中的操作均包含过滤 | |
| B. | 溶液X中ZnSO4的质量大于CuSO4的质量 | |
| C. | 步骤①中即使空气不足量,也不会导致锌的回收率降低 | |
| D. | ①产生的废气M可以用石灰乳处理,反应方程式是SO2+Ca(OH)2═CaSO4+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
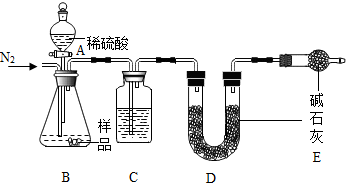 已知NaHCO3在270℃时完全分解为碳酸钠、水和二氧化碳,而Na2CO3受热不分解.现有某工厂生产出的一批NaHCO3产品中混有少量的Na2CO3,某兴趣小组同学为了测定该产品中NaHCO3的质量分数,设计了下列两种实验方案.
已知NaHCO3在270℃时完全分解为碳酸钠、水和二氧化碳,而Na2CO3受热不分解.现有某工厂生产出的一批NaHCO3产品中混有少量的Na2CO3,某兴趣小组同学为了测定该产品中NaHCO3的质量分数,设计了下列两种实验方案.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com