
| 加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
| 84 |
| x |
| 44 |
| 4.4g |
8.4g×
| ||
| 10g |
| 98 |
| 100g?y |
| 44 |
| 4.4g |
| 98 |
| 9.8g |
| 233 |
| x |
| 17.1 |
| 1.71% |
| 17.1 |
| 1.71% |
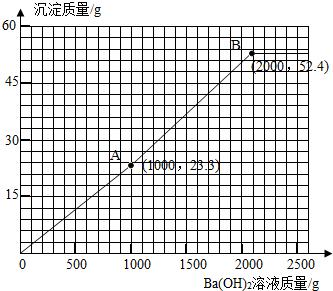
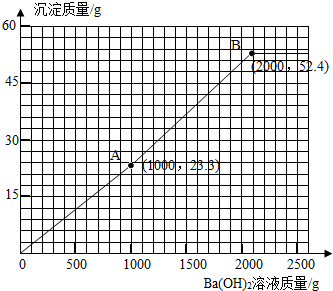


科目:初中化学 来源: 题型:
| A、10% | B、24% |
| C、12% | D、48% |
查看答案和解析>>
科目:初中化学 来源: 题型:
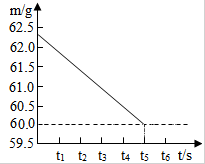 将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:
将碳酸钠和硫酸钠的固体混合物20g,放入烧杯中,再加入过量的稀硫酸220.4克,充分反应,无气体产生时,所得溶液质量为236克,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
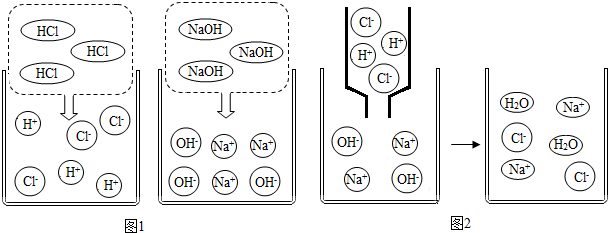
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究:
某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究:| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
| 物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
| 石蜡 | 50~70 | 300~550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、二氧化碳和一氧化碳一样都是空气污染物 |
| B、二氧化碳常被压缩冲入水中以制取各类碳酸饮料 |
| C、温室效应为人类提供了适宜的生存温度 |
| D、CO2参加光合作用可提高农作物的产量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com