
【题目】苏泊尔不锈钢锅具在近日经检测发现:制造材料不锈钢中添加锰金属含量超过国家标准。锰在不锈钢中主要起耐磨性作用,锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A.Mn + H2SO4 = MnSO4+H2↑B.Mg + MnSO4 = MgSO4+ Mn
C.Fe + MnSO4= FeSO4+ MnD.Mn + CuSO4 = MnSO4+ Cu
【答案】C
【解析】
A、锰(Mn)在金属活动性顺序中位于铝和锌之间,说明锰在金属活动性顺序里,位于氢之前,锰能与稀硫酸反应生成硫酸锰和氢气,该反应的化学方程式为:![]() ,不符合题意;
,不符合题意;
B、锰(Mn)在金属活动性顺序中位于铝和锌之间,说明锰在金属活动性顺序里,位于镁之后,镁能与硫酸锰反应生成硫酸镁和锰,该反应的化学方程式为:![]() ,不符合题意;
,不符合题意;
C、锰(Mn)在金属活动性顺序中位于铝和锌之间,说明锰在金属活动性顺序里,位于铁之前,铁不能与硫酸锰反应,符合题意;
D、锰(Mn)在金属活动性顺序中位于铝和锌之间,说明锰在金属活动性顺序里,位于铜之前,锰能与硫酸铜反应生成硫酸锰和铜,该反应的化学方程式为:![]() ,不符合题意。
,不符合题意。
故选C。


科目:初中化学 来源: 题型:
【题目】小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:请计算:

(1)20g样品中碳酸钠的质量为 g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水 g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】X,Y 两种固体溶解度曲线如图所示,下列说法正确的是
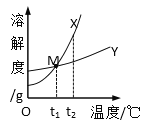
A.Y 的溶解度比X 的溶解度小
B.点M 表示 t1℃时,X、Y 的溶解度相等
C.t2℃时,X 溶液的浓度比Y 溶液的浓度大
D.将 t1℃时X 的饱和溶液升温至 t2℃,溶质的质量分数增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列各图中有关信息,回答下列问题:
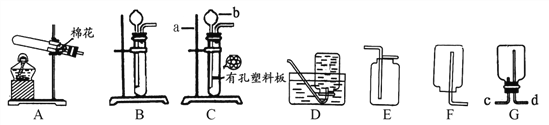
(1)仪器a、b的名称:a________,b________。
(2)若用装置A制取氧气,其反应的化学方程式_______________。若要收集到较纯净的氧气,其收集装置应选____;待收集完毕后应先_______,再________________。 某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是_________。
(3)实验制取CO2,为了控制反应的发生与停止,选择最佳的发生装置是___________;若用G装置收集CO2气体,气体应从________端(填“c”或“d”)进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】马铃薯俗称土豆、洋芋、山药蛋等,是世界第四大粮食作物,在我国种植历史已有400多年。我国是全球马铃薯产量最多的国家,约占世界总产量1/4。则:
(1)土豆是我们喜爱的一种食品,如图是土豆的主要营养成分。土豆中能为人体提供能量的营养素是______。提倡多食用土豆有利于身体健康,请你分析的理由是______________。

(2)土豆等农作物的生长需要适量的化肥。下列化肥中属于氮肥的是______(填序号)
ANH4Cl BK2CO3 CCO(NH2)2 DCa(H2PO4)2
(3)乳酸基塑料是以土豆等副食品废料为原料,经多步处理而制成的一种新型可降解塑料。下列有关乳酸基塑料的说法中错误的是________(填序号)
①土豆淀粉属于高分子化合物;②制取乳酸基塑料的原料比较低廉且广泛;③乳酸基塑料属于天然高分子材料;④乳酸基塑料易降解;⑤乳酸基塑料有助于解决白色污染问题。
(4) “可比克”薯片是用马铃薯加工的方便膨化食品,采用充气包装,可防止在运输、储存时发生挤压或变质,从经济、安全和环保的角度考虑,可充入氮气,其中的一点原因是___________。

(5)我国将逐步推进马铃薯主粮化战略,你认为未来消费马铃薯应在哪些领域进行战略性转变?(要求至少写一点)_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)豆腐是生活中常见的食品,主要成分如图所示。

(1)图中所列成分,从营养角度看,共分为_______类。
(2)除豆腐外,很多食物也能提供丰富的蛋白质。下列能提供丰富蛋白质的食品是 (填字母序号)。

(3)豆腐可以补充人体每天所需的钙元素,缺钙会导致的疾病是 (填字母序号)。
A.贫血 B.龋齿 C.骨质疏松
(4)家庭制作豆腐主要有以下的过程:①打豆浆;②将豆浆与豆渣分离;③点卤;④将豆腐花与水分离;⑤压制成块。②和④中的两次分离采取的操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如下(部分产物略去):
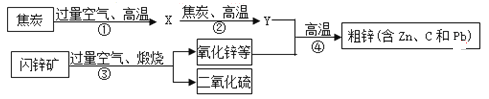
(1)X的化学式是_______,图中用过量空气的目的是_________。
(2)①~④中属于化合反应的是______。
(3)Zn______(填“能”或“不能)与PbCl2溶液反应。
(4)写出反应③中生成ZnO的化学方程式_________。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是_________。
物质 | Zn | Pb | C |
沸点℃ | 907 | 1749 | 4827 |
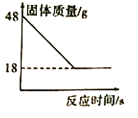
(6)反应②中固体质量随反应时间的变化图示如下图,计算产生Y的质量__________。(写出必要的计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸(HNO3)是实验室常见的一种酸,实验小组对硝酸的某些性质进行研究。
I.挥发性
(实验1)取一瓶质量分数68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到__________。
II.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3![]() 4NO2↑+O2↑+___。
4NO2↑+O2↑+___。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26 ℃)。记录溶液上方的气体颜色随时间的变化情况。
实验编号 | ① | ② | ③ |
实验条件 |
|
|
|
实验现象 | 6分钟出现浅红棕色 15分钟红棕色比较明显 30分钟红棕色非常明显 | 60分钟无明显变化 | 3分钟出现浅红棕色 6分钟红棕色比较明显 10分钟红棕色非常明显 |
(2)实验①、②对比是研究对浓硝酸稳定性的影响__________________________________。
(3)实验①、③对比可得出的结论是__________________________________________。
III.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够观察到的现象是_________________________。
IV.氧化性
(查阅资料3)浓硝酸在加热条件下能与木炭发生反应。C+4HNO3(浓)![]() 4NO2↑+ CO2↑+2H2O
4NO2↑+ CO2↑+2H2O
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有:
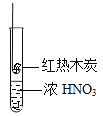
①___________________________________________________。
②___________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
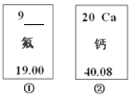
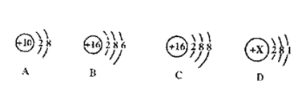
(1)氟元素的相对原子质量为_________,钙元素的原子序数(即质子数)为________;
(2)D中的X=________;
(3)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是________;表示离子的符号________
(4)B和______属于同种元素的粒子(用“A”、“C”、“D”填空)。化学性质相似的粒子____________
(5)在A、B、C、D四种粒子中,两两结合形成的物质的化学式为________________氟元素、钙元素形成化合物的化学式____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com