
【题目】过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,某实验小组在实验室用两种方法制取CaO2。
【查阅资料】
从溶液中制得的过氧化钙含有结晶水,其结晶水合物化学式为CaO2·8H2O,在140~200℃脱水干燥,即得过氧化钙成品。加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气。过氧化钙与水反应生成氢氧化钙和氧气。
【进行实验】
甲组:由鸡蛋壳(含碳酸钙高达90%)为原料最终反应制得,其制备流程如图所示,其中鸡蛋壳的预处理主要是除去碳酸钙以外的大部分杂质。
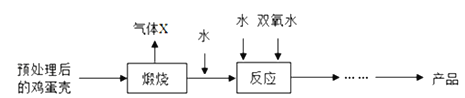
(1)气体X是__________,两次加水发生的都是化合反应,写出相关反应方程式__________,______ CaO2·8H2O,实际获得的产品不纯,主要含有的固体杂质是____________。
乙组:由氨气、双氧水、氯化钙为原料,制得CaO2·8H2O沉淀,同时产生副产品氯化氢,反应装置如图2所示。
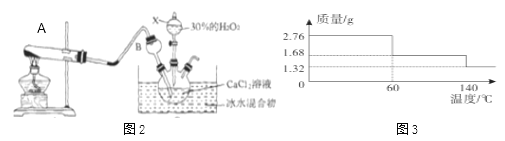
(2)装置A加热的是熟石灰和硫酸铵,写出该反应的化学方程式_____________________。
(3)制取CaO2·8H2O的化学方程式:CaCl2+H2O2+2NH3·H2O+6H2OCaO2·8H2O+2Y。则Y的化学式________,该反应一般在0~5℃的低温下进行,温度不能过高的原因是_______________。
【定性测定】
(4)产品性质测定:甲组取产品充分加热,可用_________ 检验产生的气体。乙组取产品加水,滴入无色酚酞溶液,酚酞变红,说明产品加水后生成碱性物质。若需得到同样的结论,甲组______(填“能”或“不能”)采用与乙组相同的方法。
【定量测定】
(5)2.76g CaO2·8H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140℃时完全脱水,杂质受热不分解)如图3所示。
① 试确定CaO2·8H2O样品中结晶水的质量=______g。
② 该样品中CaO2·8H2O的质量分数。(写出计算过程)_________
【交流讨论】
(6)对于上述两种制取CaO2·8H2O的方法有关评价合理的是_________(填序号)。
A.理论上甲组反应的原子利用率达100%,符合绿色化学理念
B.在原料充分转化的前提下,甲组的CaO2·8H2O沉淀过滤后不用洗涤,操作简便
C.乙组产生的副产品氯化氢可能会影响CaO2的产率
【答案】 CO2 CaO+H2O=Ca(OH)2 Ca(OH)2+H2O2+6H2O= CaO2·8H2O Ca(OH)2 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O NH4Cl 防止NH3·H2O挥发,提高原料利用率 带火星的木条 不能 1.44g 78.3% ABC
CaCl2+2NH3↑+2H2O NH4Cl 防止NH3·H2O挥发,提高原料利用率 带火星的木条 不能 1.44g 78.3% ABC
【解析】(1)根据碳酸钙在高温的条件下分解生成氧化钙和二氧化碳解答;根据两次加水发生的都是化合反应,其一是氧化钙和水反应生成氢氧化钙,其二是氧化钙和过氧化氢以及水反应生成 CaO2·8H2O解答;根据过程中氧化钙遇到了水生成氢氧化钙解答;(2)根据熟石灰和硫酸铵在加热的条件下生成硫酸钙和氨气以及水解答;(3)根据质量守恒定律分析解答;根据过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来解答;(4)根据信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”解答;根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红解答;(5)根据反应的化学方程式计算解答;(6)根据题中信息解答。(1)由于气体X是高温煅烧碳酸钙得到,所以气体X是 二氧化碳,两次加水发生的都是化合反应,其一是氧化钙和水反应生成氢氧化钙,其二是氧化钙和过氧化氢以及水反应生成CaO2.8H2O,对应的化学方程式依次为CaO+H2O═Ca(OH)2,CaO+H2O2+7H2O═CaO2·8H2O;由于过程中氧化钙遇到了水生成氢氧化钙,所以CaO2·8H2O实际获得的产品不纯,主要含有的固体杂质是 Ca(OH)2;(2)装置A加热的是熟石灰和硫酸铵,生成硫酸钙和氨气以及水,对应的化学方程式 Ca(OH)2+(NH4)2SO4![]() CaSO4+2NH3↑+2H2O;(3)制取CaO2·8H2O的化学方程式为CaCl2 + H2O2+ 2NH3·H2O+ 6H2O=CaO2·8H2O + 2Y。根据质量守恒定律可得,Y的化学式 NH4Cl;该反应一般在0~5℃的低温下进行,由于过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来,所以温度不能过高的原因是防止NH3·H2O挥发,提高原料利用率;(4)产品性质测定:甲组取产品充分加热,由于信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”,而检验氧气一般使用带火星的木条,所以可用带火星的木条检验产生的气体。乙组取产品加水,根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红,所以若需得到同样的结论,甲组能采用与乙组相同的方法;(5)由图可以看出失去的结晶水的质量为2.76g-1.32g=1.44g;
CaSO4+2NH3↑+2H2O;(3)制取CaO2·8H2O的化学方程式为CaCl2 + H2O2+ 2NH3·H2O+ 6H2O=CaO2·8H2O + 2Y。根据质量守恒定律可得,Y的化学式 NH4Cl;该反应一般在0~5℃的低温下进行,由于过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来,所以温度不能过高的原因是防止NH3·H2O挥发,提高原料利用率;(4)产品性质测定:甲组取产品充分加热,由于信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”,而检验氧气一般使用带火星的木条,所以可用带火星的木条检验产生的气体。乙组取产品加水,根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红,所以若需得到同样的结论,甲组能采用与乙组相同的方法;(5)由图可以看出失去的结晶水的质量为2.76g-1.32g=1.44g;
设样品中CaO28H2O的质量为x
CaO28H2O![]() CaO2+8H2O
CaO2+8H2O
216 144
x 1.44g![]()
x=2.16g
样品中CaO28H2O的质量分数为![]() ×100%≈78.3%
×100%≈78.3%
答:①CaO28H2O样品中结晶水的质量=1.44g;②该样品中CaO28H2O的质量分数 78.3%;(6)A、由于甲组实验中生成二氧化碳气体,之后的反应中没有二氧化碳的参与,所以甲组反应的原子利用率不是100%,错误;B、在原料充分转化的前提下,由于甲组中生成了氢氧化钙等杂质,所以甲组的CaO28H2O沉淀过滤后需要洗涤,错误;C、乙组产生的副产品氯化氢由于会和产品反应,所以可能会影响CaO2的产率,正确。故选C。


科目:初中化学 来源: 题型:
【题目】将铁粉加入足量的硫酸充分反应。
①可以看到的现象是__________________________________________________。
②下列金属中能与硫酸发生类似反应的是__________(填选项)。
A.Cu B.Mg C.Al D.Ag
(2)高温条件下
一氧化碳可把锰从四氧化三锰中还原出来,反应的化学方程式是______________________________。
1个四氧化三锰“分子”与__________个CO分子完全反应生成Mn和CO2。
(3)已知镉(Cd)的金属活动性与铁、锌相近,镉元素在化合物中常显+2价。
将镉丝插入下列溶液没有明显现象的是__________(填序号)。
①NaCl溶液 ②HCl溶液 ③AgNO3溶液 ④NaOH溶液
(4)将mg氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,得到滤渣A和滤液B。再将滤渣A加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为12.8g。原氧化铜的质量m=__________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班学生分三组分别做了二氧化碳制取和性质验证实验,如下图所示。
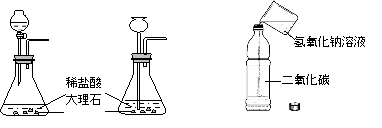
甲 乙 丙
实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合。将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。
请填空:
(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)。
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成。过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。
由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,下列说法错误的是
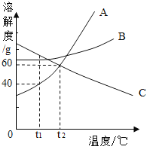
A.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和
D.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质或用品均为生活中常见。

(1)常用作调味品的是_______________(填序号,下同)。所使用的主要材料中,属于有机合成材料的是______________。
(2)生活中由于食物的腐烂变质,造成很大的浪费。
食品脱水可起到防腐保藏作用,如将蔬菜蒸干,在蒸发过程中水分子间隔___(填“增大”或“减小”).苯甲酸钠是一种常用的食品防腐剂,其化学式为C6H5CO2Na,它是由___种元素组成。铁粉常用于食品保鲜,其原因是___.
(3)能源、环境与人类的生活和社会发展密切相关。
施用化肥可以提高粮食产量,但滥用会造成环境污染。下列物质中,能用做钾肥的是___(填序号).
A.K2SO4B.CO(NH2)2C.NH4NO3D.Ca(H2PO4)2
化石燃料等不可再生能源日趋枯竭,迫切开发新能源,如氢能、___等。
(4)汽车是现代生活中不可缺少的代步工具。
汽车电路中的导线一般是用铜做的,这是利用了铜的延展性和___性;汽车如果使用天然气作燃料,对空气的污染会减小,天然气的主要成分是___;车体的主要材料为钢,是一种铁的合金,工业上用一氧化碳和赤铁矿石炼铁的反应化学方程式为___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为实验室常见的气体制备、收集等装置,按要求填空。
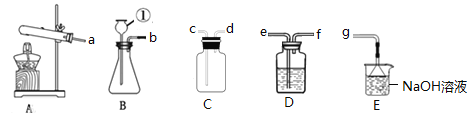
(1)写出B图中标号①仪器的名称_________;
(2)加热氯酸钾和二氧化锰的混合物制取氧气,发生装置选择_________,其中二氧化锰起_________作用;
(3)实验室若用D装置检验二氧化碳,方程式为_________;若用D装置验证二氧化碳能与水反应生成一种酸性物质,D中应盛放_________溶液(填物质名称);
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸发生复分解反应制取硫化氢(H2S)气体,写出反应的化学方程式_________;硫化氢(H2S)是一种有毒气体,密度比空气大,能溶于水形成氢硫酸,实验室常用NaOH溶液来吸收有毒的硫化氢气体,若要制取并收集一瓶硫化氢气体,选择的装置中导管的连接顺序为_________(填写
导管口标注的字母符号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酒精灯是实验室中常用的加热仪器,某兴趣小组同学对酒精灯内焰进行如下探究。
(Ⅰ)定性研究
甲同学取一根火柴梗,拿住一端迅速平放入酒精灯火焰中,1~2s后取出,观察到位于焰心的部分没有明显变化,说明焰心温度最低。
(1)写出碳完全燃烧的反应方程式______________________________。
(Ⅱ)定量研究
乙同学用注射器抽取灯芯和焰心交界处气体,利用氧气传感器测量氧气的体积分数(见下表),丙同学利用高温传感器测定酒精灯灯芯和焰心交界处温度(见下表)。
测量次数 | 第一次 | 第二次 | 第三次 |
灯芯和焰心交界处氧气体积分数 | 5.93% | 5.29% | 6.53% |
灯芯和焰心交界处温度/℃ | 236 | 243 | 240 |
(2)乙、丙同学多次进行测量的目的是_____。
(3)火柴梗燃烧需要氧气的最低含量是14.0%,着火点是270℃,结合上表谈谈你对“火柴梗在焰心处没有明显变化”的认识__________________________________。
(4)如果考虑抽气时空气的影响,则乙同学测出的氧气浓度比焰心的实际氧气浓度______。(填“高”或“低”):另外乙同学所测氧气的体积分数差异的原因可能是①_____________________;②__________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组将打印机墨盒中的墨粉倒出,发现全部是黑色粉末,于是对墨粉的成分进行下列探究:
【提出猜想】该粉末可能含有炭粉、铁粉、氧化铁、四氧化三铁中的一种或几种。
(1)小明认为不可能含有氧化铁,原因是 __________________
【查阅资料】①四氧化三铁具有磁l生,能被磁铁吸引;
②金属氧化物能溶于稀酸。

______________
【进行实验】
(2)用化学方程式表示实验③中澄清石灰水变浑浊的原因________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的食盐水里,经发酵而成。
(1)现要配制50克的氯化钠溶液,实验用品如下图,其中还缺少的玻璃仪器是_____________。

实验步骤如下:
①计算
②称量:若将物品和砝码放反,则实际称得NaCl质量为___________g。(1g以下用游码)
③量取:用__________(填“10”、“50”或“100”)mL量筒量取水。
④溶解
(2)下列操作一定能导致氯化钠溶液的溶质质量分数偏小的是__________(填序号)。
①称量时,天平指针左偏 ②量取水时仰视读数
③溶解时,未用玻璃棒搅拌 ④装瓶时,有部分溶液洒出
(3)泡好泡菜的关键之一是密封性要好,这样才有助于泡菜水发酵。其中,发酵的过程_________(填“属于”或“不属于)缓慢氧化。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com