
| |||||||||||||||||||
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
| 实验 | 实验步骤 | 实验现象 |
| ① | 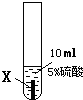 |
X片表面无明显变化 |
| ② | 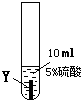 |
Y片表面无明显变化 |
| ③ | 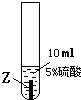 |
Z片溶解,表面有无色氢气产生,溶液最终为无色 |
| 实验 | 实验步骤 | 实验现象 |
| ④ | 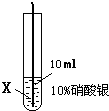 |
在X丝表面有银白色的固体析出 |
| ⑤ |  |
在Y丝表面没有明显现象 |
| 实验编号 | 硫酸的质量分数/% | 反应的温度 | Z丝消失的时间/S |
| ⑥ | 3 | 20 | 500 |
| ⑦ | 6 | 20 | 300 |
| ⑧ | 6 | 30 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
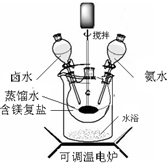 碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.
碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.| 实验操作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸. ②再向上述所得溶液加 硝酸银或AgNO3 硝酸银或AgNO3 溶液 |
现象① 产生气泡 产生气泡 ;现象② 产生白色沉淀 产生白色沉淀 ; |
含有 Cl- |
| ||
查看答案和解析>>
科目:初中化学 来源:番禺区一模 题型:问答题
| 实验 | 实验步骤 | 实验现象 |
| ① | 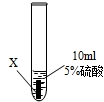 |
X片表面无明显变化 |
| ② | 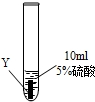 |
Y片表面无明显变化 |
| ③ | 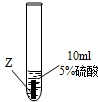 |
Z片溶解,表面有无色氢气产生,溶液最终为无色 |
| 实验 | 实验步骤 | 实验现象 |
| ④ | 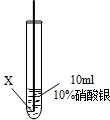 |
在X丝表面有银白色的固体析出 |
| ⑤ | 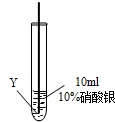 |
在Y丝表面没有明显现象 |
| 实验编号 | 硫酸的质量分数/% | 反应的温度 | Z丝消失的时间/S |
| ⑥ | 3 | 20 | 500 |
| ⑦ | 6 | 20 | 300 |
| ⑧ | 6 | 30 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:
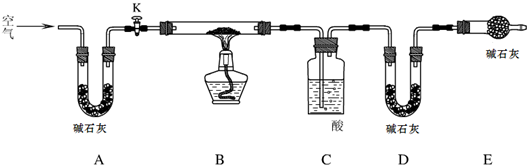
某同学设计实验,用Zn和稀硫酸制H2并用干燥的氢气还原CuO
①写出仪器名称:x是 ,y是 ,z是 ;
②排出该同学实验时的装置顺序 ;
③若只提供给该同学Zn粒和浓盐酸,实验应证明并除去杂质,改进后,排出仪器接口顺序 ;
④证明杂质的现象是 ;
依据的化学方程式是 。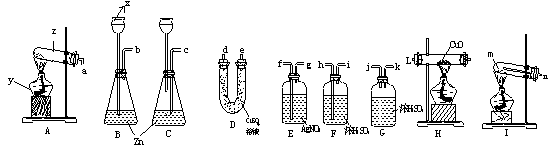
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com