
【题目】镓是一种奇妙的金属,放在手心马上融化,犹如荷叶上的水珠流来流去。结合如图信息判断下列说法不正确的是( )
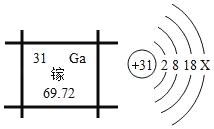
A. 图中X=3
B. 金属镓的熔点很低
C. 镓的氧化物的化学式为Ga2O3
D. 镓元素在周期表中与氮元素是同一族
科目:初中化学 来源: 题型:
【题目】某物质在空气中燃烧的化学方程式为2X+3O2![]() 2CO2+4H2O,下列说法正确的是( )
2CO2+4H2O,下列说法正确的是( )
A. O2中氧元素的化合价为﹣2
B. 该反应属于置换反应
C. X属于有机物
D. CO2中碳、氧元素的质量比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量的a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图1;然后升温到50℃时,现象如图2;a、b两种物质的溶解度曲线如图3.由这一过程可知( )
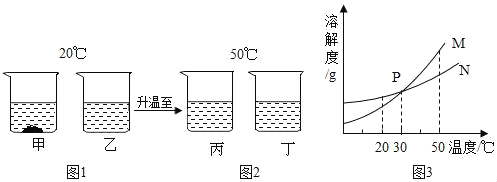
A. 30℃时a、b溶液溶质质量分数不相等
B. 40℃时a、b溶液溶质质量分数大小无法比较
C. 从20℃到50℃,b溶液质量分数不变
D. 图3中表示a的溶解度曲线是N
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验:称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生产的气体与所加稀硫酸的质量关系如图所示。求:
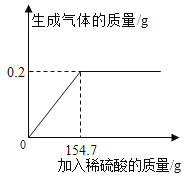
(1)黄铜样品中锌的质量
(2)恰好完全反应时,所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 某固体物质可能含有硫酸钠、碳酸钠、氯化钙、硫酸铜和氢氧化钾中的一种或几种。为探究其组成,进行如下实验,流程和现象记录如下:【资料】氯化钙、氯化钡、氯化钾三种溶液均呈中性
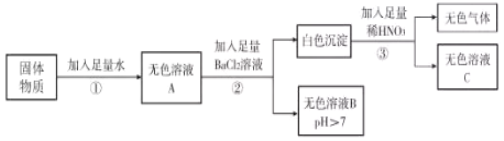
(1)依据步骤①的实验现象得出固体物质中一定不含 (填化学式)。
(2)步骤②中发生反应的化学方程式为 。
(3)根据上述实验得出固体物质中一定含有 (填化学式,下同),可能含有 。为进一步确定可能含有的物质,采用的方法是 (写出实验的操作、现象和结论)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
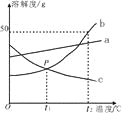
(1)P点表示在t1℃两物质的溶解度关系为b c(填“>”、“<”或“=”)。
(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为 。
(3)t2℃时,50 g b物质加入到50 g水中充分溶解后,所得溶液的质量为 。
(4)b中含有少量的a,若要提纯b,可采用 结晶的方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对中和反应进行如下研究:
(1)甲同学按下图进行实验,证明了盐酸和NaOH溶液能发生化学反应,他依据的实验现象是_______,写出该反应的化学方程式_________。
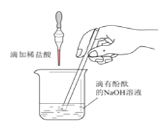
(2)乙同学依据下图,认为甲同学实验无法确定酸碱恰好完全反应,其分析的原因是______。
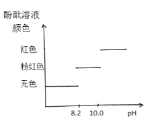
(3)丙同学用传感器测稀盐酸和NaOH溶液反应过程中的pH变化,测定结果如图。请判断40s时,溶液中溶质的成分为_________。
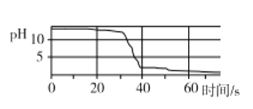
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在食盐中加入适量的碘酸钾(KIO3),可预防碘缺乏病。
(1)人类膳食中缺碘易患_________
A 甲状腺肿大 B 贫血 C 骨质疏松症 D 软骨病
(2)某兴趣小组的同学,欲检测一袋食盐是否为加碘食盐,他们查阅资料得知,加碘食盐中的KIO3在酸性条件下能与KI溶液发生反应,生成碘(I2),淀粉遇I2变蓝色。现提供下列试剂和生活中常见的物质:
①KI溶液;②纯碱:③米汤;④白糖;⑤白酒:⑥白醋,该小组同学进行实验必须选用的试剂和物质是_______________
A ①③④ B ①③⑥ C ②④⑥ D ①④⑤
(3)该小组同学仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行探究。
问题一:食盐是比较稳定的,而说明中强调“防热”,是否因为受热会造成碘的损失?
(实验一)探究温度对碘损失率的影响
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸
钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
①分析上表可得出的结论是_____________________________________
②人们常说:“炒菜时要后放碘盐,以免碘的损失。”这里的“碘”指的是____(填“碘单质”、“碘 元素”或“碘原子”)。
问题二:炒菜时加醋对碘的损失率是否也有影响?
(实验二)探究酸碱度对碘损失率的影响
③此组对照实验,要控制在加热的时间和温度、碘酸钾溶液的浓度和______均相同,溶液的酸碱度不同的条件下进行。
④实验需要调节溶液的酸碱性,下列物质不能选用的是_______(填字母)。
A 氢氧化钠 B 纯碱粉末 C 食盐晶体 D 稀盐酸
(4)碘酸钾中碘元素的质量分数为______。我国规定,食盐中加碘的含量为每千克食盐含腆0.035克,相当于每千克食盐含碘酸钾_____克。(精确到小数点后二位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com