
【题目】图1为利用气压传感器测定红磷燃烧时集气瓶内气压变化的实验装置。点燃燃烧匙内的红磷后,立即伸入集气瓶中并把塞子塞紧,待红磷熄灭并冷却后,打开止水夹。集气瓶内气压的变化情况如图2。下列说法不正确的是
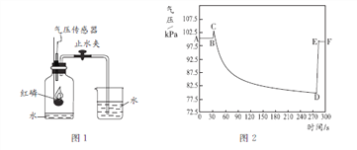
A. BC段气压增大的主要原因是燃烧放热
B. CD段气压减小的主要原因是集气瓶内氧气不断被消耗
C. DE段气压增大的主要原因是烧杯中水进入集气瓶后,气体体积减小
D. 若用木炭代替红磷完成此实验,集气瓶内气压变化趋势与图2基本一致
科目:初中化学 来源: 题型:
【题目】某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。
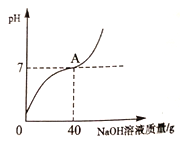
(1)图中A点表示的意义是____________________。
(2)A点消耗氢氧化钠溶液的溶质的质量为___________g。
(3)求石油产品中残余硫酸的质量___________g(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
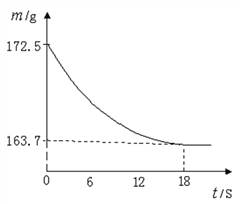
求:(1)生成CO2的质量为__________g。
(2)该纯碱样品中Na2CO3的质量分数为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
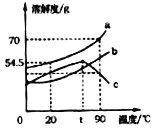
A. a属于易溶性物质
B. t℃时c物质的饱和溶液,可采用升高温度方法使其变为不饱和溶液
C. 90℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的饱和溶液
D. 将20℃时三种物质的饱和溶液升温到90℃,所得溶液中溶质的质量分数的大小关系是:a>c>b
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年12月28日,全球首段承载式太阳能光伏发电公路试验段在我省建成通车。高纯硅是光伏发电的重要材料,生产高纯硅的流程图如图:

(1)生产高纯硅需要对普通石英砂(含有少量Fe2O3杂质)进行提纯,其中酸洗是一个重要的步骤。请写出用盐酸除去Fe2O3的化学方程式_____。
(2)整个生产过程中必须控制无氧、无水。在HSiCl3与H2反应过程中若混入O2,可能引起的后果是_____。HSiCl3遇水能剧烈反应生成H2SiO3、H2与HCl,该反应的化学方程式是_____。
(3)为了节约资源,上述生产流程中可循环利用的物质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。
Ⅰ.挥发性
(实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到________,是由于挥发出来的硝酸蒸体遇到空气里的水蒸气形成硝酸小液滴的缘故。
Ⅱ.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3 ![]() 4NO↑+O↑+_____。
4NO↑+O↑+_____。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。
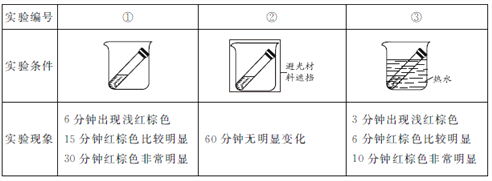
(2)实验①、②对比是研究______对浓硝酸稳定性的影响。
(3)实验①、③对比可得出的结论是_______。
Ⅲ.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够看到的现象是_______。
IV .氧化性
(查阅资料3) 浓硝酸在加热条件下能与木炭发生反应:C+4HNO(浓) ![]() 4NO↑+CO↑+2H2O。
4NO↑+CO↑+2H2O。
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂排出的废水溶质可能由硫酸钠、碳酸钠、氯化钠、氢氧化钠中的一种或多种组成,为确认其组成,某化学实验小组进行了如下两组实验。
实验一 | 实验二 | ||||
步骤 | 试剂 | 现象 | 步骤 | 试剂 | 现象 |
① | 取少量废水于烧杯 | / | ① | 取少量废水于烧杯 | / |
② | 滴入少量酚酞 | —— | ② | 滴入过量 | 产生沉淀 |
③ | 继续滴加过量稀盐酸 | 产生气体 | ③ | 过滤得滤液和滤渣 | / |
④ | 继续滴加少量 | 产生沉淀 | ④ | 向滤液中滴入少量酚酞 | 无明显现象 |
⑤ | 过滤取滤液 | / | ⑤ | 继续滴少量 | 产生沉淀 |
⑥ | 向滤液中滴少量 | 无沉淀 | ⑥ | 向滤渣中滴过量稀盐酸 | 沉淀消失 |
根据上述两组实验及其现象,回答下列问题:
(1)实验一步骤②所对应的现象为_____________________________________。
(2)实验一步骤③产生气体的反应的化学方程式为________________________
(3)废水中一定无_________(填化学式,下同),可能有_________________
(4)媛媛为进一步确认废水组成,另取废水进行定量实验,测得其中阳离子与阴离子的个数比约为4:3,由此可知原废水溶质为______________。
(5)实验二为相同实验目的,酚酞可用下列试剂_____(填序号)中任意一种替换。
A.铁粉 B.硝酸铜溶液 C.紫色石蕊 D.稀硝酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生存与发展离不开化学.
(1)2017年5月,我国首架大型客机C919首飞,飞机材料中使用了大量的铝镁合金,铝制品具有“自我保护”能力,原因是____________________________。
(2)2017年5月,我国在南海进行了可燃冰的试开采并获得成功,天然气的主要成分为________ (填化学式),其完全燃烧的化学方程式为______________________。
(3)活性炭净化水,是利用了它的______性,生活中硬水软化的常用方法是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】由我国化工专家侯德榜探索发明的“侯氏制碱法”,其生产过程涉及的主要化学反应如下:①NH3+CO2+X=NH4HCO3 ②NH4HCO3+NaCl(饱和)==NH4Cl+NaHCO3 ↓ ③2NaHCO3![]() Na2CO3+H2O+CO2 ↑ 请回答:
Na2CO3+H2O+CO2 ↑ 请回答:
(1)反应①中X的化学式为___________________;
(2)反应②属于基本类型中的____________________反应。
(3)除去混在Na2CO3粉末中少量的NaHCO3的方法是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com