
 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:分析 (1)根据蜡烛能浮在水面上,比较蜡烛和水的密度;
(2)根据温度越高,火柴梗易被炭化分析;
(3)根据蜡烛燃烧的产物以及白烟的成分分析.
解答 解:(1)由于蜡烛浮在水面上,说明石蜡的密度比水小;
(2)由于温度越高,火柴梗易被炭化.所以,看到火柴梗的a处最先变黑,说明蜡烛火焰的外焰温度最高;
(3)由题意可知,由烧杯内壁出现水雾,说明了蜡烛燃烧生成了水;由澄清的石灰水变浑浊,说明了蜡烛燃烧生成二氧化碳;
结论:蜡烛燃烧时生成了水和二氧化碳
故答案为:(1)小;(2)a,外焰;(3)水雾,浑浊,水和二氧化碳.
点评 本题主要测试学生的实验操作能力和方法的掌握情况,以及学生对石蜡的性质的了解,如果学生了解石蜡的成分,并能正确分析实验现象,就能正确解答.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
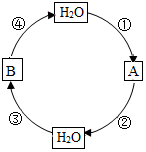 水与人类的生活和生产密切相关.请回答以下问题:
水与人类的生活和生产密切相关.请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
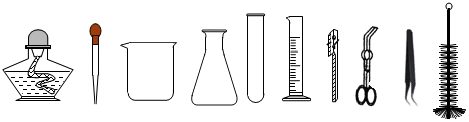
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
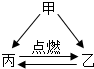 甲、乙、丙是初中化学中常见的三种不同类别的物质,其中乙是水,它们之间的转化关系如图所示.“→”表示由一种物质转化成另一种物质(图中部分反应条件及物质略去).
甲、乙、丙是初中化学中常见的三种不同类别的物质,其中乙是水,它们之间的转化关系如图所示.“→”表示由一种物质转化成另一种物质(图中部分反应条件及物质略去).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
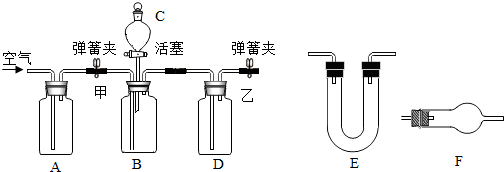
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com