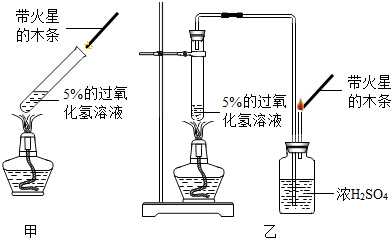
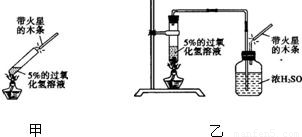
解:(1)由于过氧化氢溶液中含有很多的水,制取的氧气中也会含有大量的水蒸气,导致甲中除了生成O
2外还有较多的水蒸气,而乙装置加了干燥装置,降低了水蒸气的含量.由于含氧气浓度大带火星的木条才容易复燃.
①实验室制取氧气常用过氧化氢溶液与催化剂(二氧化锰),反应原理为2H
20
2
2H
2O+0
2↑.
②乙装置将生成的氧气通过浓硫酸,使氧气中的水蒸气除去了.
(2)①氧气能供给呼吸和支持燃烧,需要氧气的例子是人工呼吸、燃烧.
②食物在氧气中因缓慢氧化而变质,灯泡中的钨丝会因为氧化而不能发光,因此隔绝氧气的例子有灯泡中的钨丝、真空保存食物.
故答案为:(1)①2H
2O
2
2H
2O+O
2↑
②除去H
2O
2溶液加热时产生的水蒸气
(2)①人工呼吸,燃烧
②灯泡中的钨丝,真空保存食物
分析:(1)实验室用加热5%的过氧化氢方法制取氧气,由于氧气中含有的水分多,带火星的木条不复燃.图乙将制得的氧气通过浓硫酸水蒸气除去,带火星的木条复燃.
(2)根据氧气的供给呼吸和支持燃烧的性质回答.
点评:只有含氧气的浓度达到一定值时,才容易使带火星的木条复燃,如果不易复燃说明氧气的浓度小.


 2H2O+02↑.
2H2O+02↑. 2H2O+O2↑
2H2O+O2↑