
【题目】自然界中的碳循环。
碳是组成生物体的基本元素之一,也是组成煤、石油、天然气的主要元素之一,自然界中的碳循环主要是通过CO2来实现的,如图是碳循环主要途径的模式图。
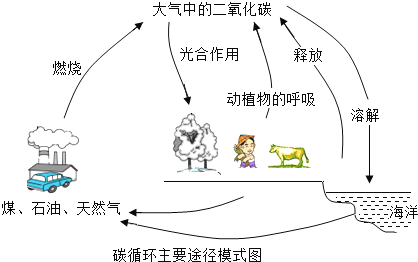
(1)结合图,下列关于碳循环的认识正确的是(填序号)_____。
A有机物和无机物可以相互转化
B碳循环过程只涉及到化学变化
C碳循环过程中,各元素的化合价都不变
D燃烧过程中能量的转化形式是化学能转化为热能和光能
(2)用化学方程式表示图中碳循环中的下列变化
①动物体内的葡萄糖在酶的作用下发生缓慢氧化,生成二氧化碳和水_____。
②消耗二氧化碳的一种方式_____。
(3)从化学的视角看物质
目前,人们对二氧化碳的评论褒贬不一,请列举有力的证据取论证褒贬两方面的观点。
要求:①表达完整,因果关系清晰明确 ②一个角度举出一个事例即可③字数分别控制在30字内。
有益处:_____;
有害处:_____。
【答案】AD C6H12O6 +6O2![]() 6CO2+6H2O CO2+H2O=H2CO3 二氧化碳可以促进绿色植物的光合作用,因此可以做气体肥料;二氧化碳可以做化工原料,用于生产尿素、纯碱、制碳酸饮料等;二氧化碳可以制干冰,用于人工降雨或人造云雾等;二氧化碳既不能燃烧,也不能支持燃烧,因此可以灭火 二氧化碳无毒,二氧化碳不供给呼吸,所以可以使人窒息死亡;二氧化碳增多,引起温室效应
6CO2+6H2O CO2+H2O=H2CO3 二氧化碳可以促进绿色植物的光合作用,因此可以做气体肥料;二氧化碳可以做化工原料,用于生产尿素、纯碱、制碳酸饮料等;二氧化碳可以制干冰,用于人工降雨或人造云雾等;二氧化碳既不能燃烧,也不能支持燃烧,因此可以灭火 二氧化碳无毒,二氧化碳不供给呼吸,所以可以使人窒息死亡;二氧化碳增多,引起温室效应
【解析】
(1)A、生物圈中的碳循环主要表现在绿色植物从空气中吸收二氧化碳,经光合作用转化为葡萄糖,并放出氧气,有机物和无机物可以相互转化,故正确;
B、生物圈中的碳循环主要表现在绿色植物从空气中吸收二氧化碳,经光合作用转化为葡萄糖,并放出氧气有新物质生成,属于化学变化,
不是碳循环过程只涉及到化学变化,故错误;
C、碳循环过程中,有单质氧气生成,氧元素的化合价改变,故错误;
D、燃烧过程中能量的转化形式是化学能转化为热能和光能,故正确。
故答案:AD
(2)①生物体内的葡萄糖(C6Hl2O6)被缓慢氧化生成二氧化碳和水,反应的化学方程式为:C6H12O6 +6O2![]() 6CO2+6H2O。
6CO2+6H2O。
②二氧化碳与水反应生成碳酸,反应的化学方程式为:CO2+H2O=H2CO3;
(3)观点一:二氧化碳的“利”大于“弊”;观点二:二氧化碳既有“利”也有“弊”;观点三:二氧化碳的“弊”大于“利”
论据①:有益处:
A、二氧化碳可以促进绿色植物的光合作用,因此可以做气体肥料;
B、二氧化碳可以做化工原料,用于生产尿素、纯碱、制碳酸饮料等;
C、二氧化碳可以制干冰,用于人工降雨或人造云雾等;
D、二氧化碳既不能燃烧,也不能支持燃烧,因此可以灭火;
论据②:弊:
A、二氧化碳无毒,二氧化碳不供给呼吸,所以可以使人窒息死亡;
B、二氧化碳增多,引起温室效应。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】请用化学用语填空:
(1)氩的元素符号_____。
(2)两个亚铁离子_____。
(3)标出碳酸钾中碳元素的化合价_____。
(4)地壳中含量最多的元素_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g。某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图9所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O。请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计算过程,结果精确到0.001)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与能源开发
氢能源是理想能源,氢能源开发一直是前沿科学研究的课题之一。科学家研发出一种以铝镓合金(镓:Ga)和水为原料制取氢气的新工艺,流程如图2所示:
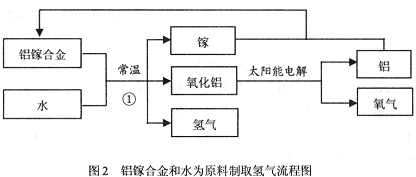
(1)从物质分类的角度看,铝镓合金属于(填“混合物”或“纯净物” ,用该合金与铝片相互刻划,发现铝片上有划痕,说明 。
(2)氢气是一种能源,它在空气中燃烧的化学方程式 。氢气被称为“绿色能源”的主要原因是 。
(3)反应①中镓的作用是 ,该反应的化学方程式 是 ,
属于四种基本反应类型中的 。与电解水制取氢气相比,用铝镓合金和水为原料制取氢气的优点是 (答出一点即) 。
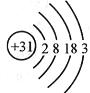
(4)镓的原子结构示意图如图所示,请写出镓与稀盐酸反应的化学方程式 ,发生有效相互作用的微粒的转化过程是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钙片的标签如图所示,且钙片中只有碳酸钙中含有钙元素。为测定其真实的含钙量,小东取10片钙片放入盛足量盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量。
小东做了三次实验,数据如下表:
物质的质量/ g | 第一次 | 第二次 | 第三次 | 平均值 |
反应前:烧杯+盐酸 | 22 | 22 | 22 | 22 |
10片钙片 | 8 | 8 | 8 | 8 |
反应后:烧杯+剩余物 | 26.7 | 26.5 | 26.9 | 26.7 |
(1)请列式计算每片此钙片含碳酸钙的质量_______。
(2)请通过计算说明此标签中的含钙量是否合理_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】原水(未经处理的水)中含有泥沙、悬浮物和细菌等杂质。在水中洒些明矾,可除去水中的泥沙、悬浮物,使水澄清,可用次氯酸杀死细菌。氯气溶解于水时,可生成盐酸和次氯酸。某水厂生产自来水的净化步骤如下:
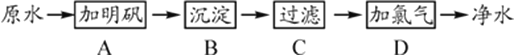
(1)可以除去大颗粒悬浮物杂质的步骤是_____。(填标号)
(2)能消毒杀菌的步骤为_____。(填标号)
(3)A步中加明矾的作用为_____。
(4)该厂生产的自来水是_____(填“纯净物”或“混合物”),其原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品13.4 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。
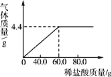
(1)当加入稀盐酸40.0 g时,所得溶液中溶质的成分是______________(写化学式)。
(2)恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1﹪)___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com