
| 65 |
| x |
| 161 |
| y |
| 2 |
| 0.2g |
| 98 |
| z |
| 16.1g |
| 103.5g-3.5g |


科目:初中化学 来源: 题型:
| A、对苯二胺中碳元素的质量分数最大 |
| B、对苯二胺的相对分子质量为27 |
| C、对苯二胺中含有两个氮原子 |
| D、对苯二胺中碳、氢、氮元素的质量比为3:4:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 温度(℃) | 0 | 20 | 60 |
| Ba(OH)2溶解度(g) | 1.67 | 3.89 | 20.94 |
| Ca(OH)2溶解度(g) | 0.189 | 0.173 | 0.121 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | NaC1 | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量的气泡 | 该溶液是 相关的化学方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
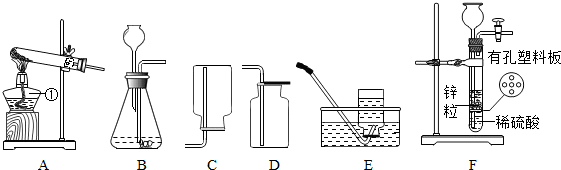
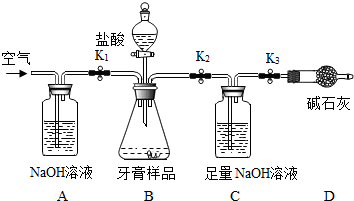
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

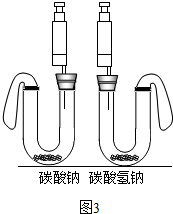
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加足量 | 剩余的固体有Na2CO3 | |
| 静置,继续滴加酚酞 | 不变红 | 剩余的固体没有NaOH |
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com