
【题目】为了探究燃烧的条件,某兴趣小组的同学设计如下实验:实验装置如下图所示,在250 mL烧杯中,注入200 mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷的着火点为40℃,红磷的着火点为200℃)。不一会儿,观察到:
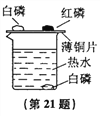
(1)铜片上的白磷燃烧起来,这是因为白磷具有_______,温度达到_______且又与_______接触。铜片上的红磷不燃烧,这是因为红磷虽然与_______接触,但温度没有达到_______。水中的白磷不燃烧,这是因为水中白磷温度虽超过_______,却不与_______接触。
(2)若铜片上白磷的量比较多,燃烧一段时间后,铜片上的红磷也会燃烧起来,为什么?__________________________________________。
(3)白磷燃烧应该出现的现象是什么?____________________________。
(4)若将烧杯上的铜片移走,并用一根玻璃导管对着水中的白磷吹入空气。你将观察到什么现象?为什么?___________________________________。
【答案】 可燃性 着火点 氧气 氧气 着火点 40℃ 氧气 白磷燃烧放出热量,使温度达到了红磷的着火点 放出热量,产生大量的白烟 水中白磷燃烧,白磷与氧气接触且温度达到了白磷的着火点
【解析】(1)铜片上的白磷能够燃烧,是因为具备了物质燃烧的条件:①物质具有可燃性.②可燃物与氧气接触.③达到可燃物的着火点;而红磷虽与氧气接触,但由于红磷的着火点高,温度未到到着火点,故不能燃烧;水中的白磷不燃烧,这是因为水中白磷温度虽超过着火点,却不与氧气接触。(2)白磷量比较多,燃烧一段时间后铜片以及红磷周围的温度升高,达到了红磷的着火点.红磷又与氧气接触,符合物质燃烧的条件.所以红磷也燃烧了起来;燃烧的方程式为:4P+5O2![]() 2P2O5;(3) 白磷燃烧应该出现的现象是:剧烈燃烧,放出大量热,产生大量白烟;(4)水中的白磷开始不能燃烧,就是因为没与氧气接触.现在用导管对着水中的白磷吹入空气,可以看到白磷在水中燃烧,因为热水中的温度超过了白磷的着火点,吹入空气,使白磷与空气中的氧气接触,满足了白磷燃烧的条件;燃烧的现象为:发出黄光,产生大量白烟。
2P2O5;(3) 白磷燃烧应该出现的现象是:剧烈燃烧,放出大量热,产生大量白烟;(4)水中的白磷开始不能燃烧,就是因为没与氧气接触.现在用导管对着水中的白磷吹入空气,可以看到白磷在水中燃烧,因为热水中的温度超过了白磷的着火点,吹入空气,使白磷与空气中的氧气接触,满足了白磷燃烧的条件;燃烧的现象为:发出黄光,产生大量白烟。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:初中化学 来源: 题型:
【题目】将一种白色固体A和一种黑色固体B按一定比例混合后加热,产生一种无色无味的气体C;取淡黄色粉末D点燃放入气体C中,会产生蓝紫色火焰,生成一种有刺激性气味的气体E。试回答:
(1)A、B、C、D、E各是什么物质?
A________,B________, C________,D________,E________。黑色粉末B在A的分解反应中起___________作用。
(2)写出上述有关反应的文字表达式:_______________, _____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛因为有神奇的性能越来越引起人们的关注。常温下钛不与非金属及强酸反应,加热时却可以和常见的非金属单质反应。钛是航空、军工、电力等工业领域的重要原材料。地壳中的钛矿石之一是金红石(主要成分是TiO2),目前大规模生产钛的方法是:
(1)使金红石与炭粉混合,在高温条件下反应,再通入氯气,制得TiCl4和一种可燃性气体。该反应的化学方程式是_____________________。
(2)在氩气的气流中,高温下用过量的镁和TiCl4反应可制得金属钛。写出该反应的化学方程式:___________________________________。
(3)从上述反应的混合物中分离出金属钛。写出简单的分离步骤和有关的化学方程式。_____________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂欲从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
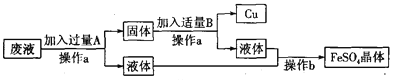
(1)操作a、b的名称分别是_______、_______。
(2)写出流程中有关反应的化学方程式:_______、_______。以上两个反应能够发生的原因是____________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分) 分类就是按照种类、等级或性质分别归类。依据不同的分类标准,结论也不尽相同。下列每组中有一种物质具有特殊的组成或性质,而其他两种物质的组成或性质相似。请你利用所学知识将其区分出来并说明理由。
化学式 | 被区分的物质(名称) | 理由 |
CO2、CO、H2O | ||
Na、NaOH、Na2CO3 | ||
HCl、H2SO4、H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法不正确的是 ( )

A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为86.4 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
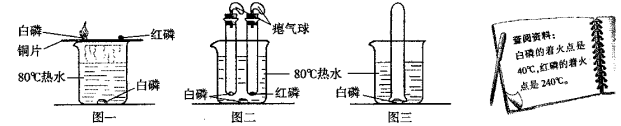
【知识回忆】可燃物燃烧的必备条件是 ;
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成H2和一种碱(化学式为KOH),该反应是 (填“吸热”或“放热”)反应,其反应化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室常用甲酸(CHOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH![]() CO↑+H2O.下图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.
CO↑+H2O.下图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.
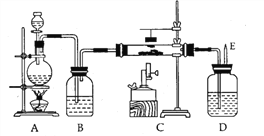
(1)先检查装置的气密性,实验开始应检验______________,以防爆炸.
(2)装置B中盛放_________,除去__________________;
(3)装置D中盛放____________,检验______________________;
(4)写出装置C中反应的化学方程式______________________;
(5)实验结束时应先停止___________处加热;
(6)在反应后磁铁悬在玻璃管上方,其中的作用是__________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白.
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂.
【实验验证】
实验步骤 | 实验现象 | 实验结论 | |
实验一 | _______________ | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中 | ________ | 氧化铝能加快过氧化氢的分解速率 |
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究_______________________________________ 。
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行__________,洗涤,干燥,称量;④对比反应前后氧化铝的质量.
【交流讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究_____________________________________ 。
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铝对过氧化氢溶液分解的催化作用,其中观察效果最差的_________
|
|
|
|
第一组 | 第二组 | 第三组 | 第四组 |
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com