
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入 硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条伸入氧气中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色氧化铜变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应放热 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、依据未打磨的铝条表面存在氧化铝的保护膜分析解答;
B、依据氧气的性质分析解答即可;
C、依据一氧化碳的化学性质分析解答即可;
D、将氢氧化钠固体加入水中,溶液温度升高,说明氢氧化钠溶于水放热.
解答 解:A、未打磨的铝条表面存在氧化铝的保护膜从而阻碍了铝与硫酸铜的反应,所以不能说明铝不如铜活泼,故选项错误;
B、将带火星的木条伸入氧气中木条能够复燃,说明了氧气具有助燃性,也就是氧气能支持燃烧,故选项正确;
C、将CO通过灼热的氧化铜黑色氧化铜变成红色,说明该过程生成了铜,从而说明CO具有还原性,故选项错误;
D、将氢氧化钠固体加入水中,溶液温度升高,说明氢氧化钠溶于水放热,但该过程是物理变化,故不能说反应,故选项错误;
故选项为:B.
点评 本题通过实验过程和实验现象进行分析,得出正确的结论,同学们要结合物质的性质前后结合仔细分析,才能得出正确的答案.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
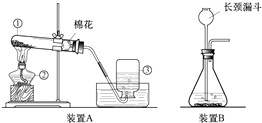
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
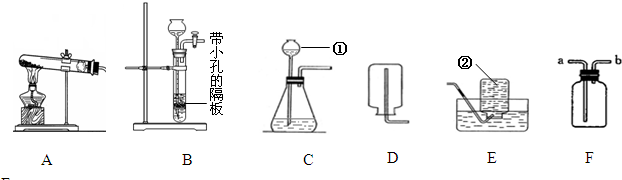
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
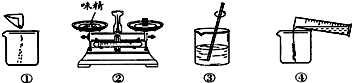
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com