
| | Zn(OH)2 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
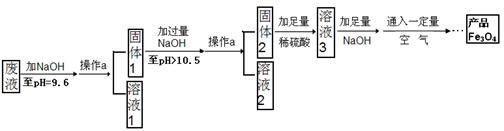


科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验步骤 | 实验现象 | 结论 |
| A.取少量滤液加入过量的BaCl2溶液中 | 产生白色沉淀 | 一定有 |
| B.将A中的混合物过滤,向滤液中加入 | | 一定有NaOH |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 |
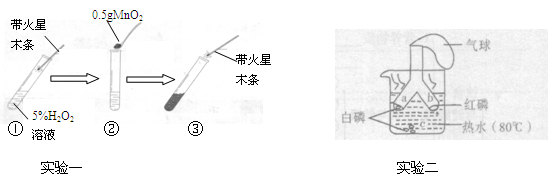
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿 | |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 | |
| ③向操作②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
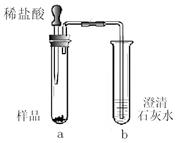
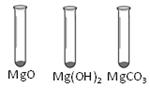
| | MgO | Mg(OH)2 | MgCO3 |
| 消耗稀盐酸的体积 /mL | 10.4 | 7.2 | 5.0 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.小明用木炭代替红磷做测定空气中氧气含量的实验 |
| B.小颖用锌、铁、铜和稀盐酸确定锌、铁、铜三种金属的活动性 |
| C.小聪在20℃配制36%的氯化钠溶液(20℃时氯化钠的溶解度为36 g) |
| D.小青将过量的木炭粉和少量氧化铜粉的混合物置于蒸发皿里加强热,得到纯净的铜 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 溶解度(20℃) | ﹤0.01g | 0.01g~1g | 1g~10g | ﹥10g |
| 物质分类 | 难溶 | 微溶 | 可溶 | 易溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com