
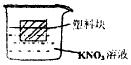
A.变大 B.变小
C.不变 D.三种情况均有可能
科目:初中化学 来源: 题型:
 (2012?金牛区一模)如图是甲乙两种固体物质的溶解度曲线.据图回答:
(2012?金牛区一模)如图是甲乙两种固体物质的溶解度曲线.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:
 KNO3和KCl在不同温度时的溶解度如下表所示.
KNO3和KCl在不同温度时的溶解度如下表所示.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
| A.升温 | B.降温 | C.加溶质M |
| D.加水 | E.加另一种固体N | F.恒温蒸发水 |
| G.与t℃时M的饱和溶液混合 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
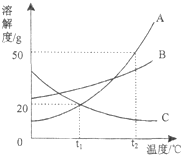 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com