
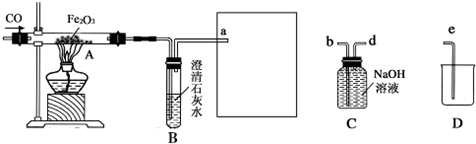
分析 (1)根据一氧化碳的密度比水小分析解答;
(2)根据一氧化碳易可燃,容易发生爆炸考虑;
(3)根据实验现象的描述和方程式的书写方法考虑.
解答 解:(1)一氧化碳需要从d端进去,从b端将溶液排出,连接e,将排出的液体排到D中,故填:d,b,e;
(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;故填:赶尽玻璃管内的空气,防止加热时爆炸;
(3)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,所以现象是红色固体变为黑色,反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:红色固体变为黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 预期的实验现象 | 结论 |
| ①用磁铁充分接触滤纸上的脱氧剂粉末; ②将红色物质放入小试管中,加入足量稀硫酸观察现象.继续滴加足量的NaOH溶液. | 绝大部分黑色粉末被吸引 红色物质溶解,溶液呈黄色,产生红褐色沉淀 | 脱氧剂的成分是铁粉 红色物质是Fe203 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若A.C是单质,B.D是化合物,则该反应一定是置换反应 | |
| B. | 若A是可溶性碱,B是可溶性盐,则C.D可能是两种沉淀 | |
| C. | 若生成物C、D分别是盐和水,则反应物A、B一定是酸和碱 | |
| D. | 若A、B各取10g混合,使其充分反应,则C、D质量的总和不一定等于20g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝和硫酸铜溶液 | B. | 氯化钠溶液和稀硫酸 | ||
| C. | 把二氧化碳通入澄清的石灰水 | D. | 碳酸钙固体和稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com