
| A. | 将氢氧化钠固体加入水中,温度会将会降低 | |
| B. | 用硬水洗衣服不如用软水洗得干净 | |
| C. | 硝酸铵溶于水制得的冰袋可用于给高烧病人降温 | |
| D. | 冬季向公路上的积雪撒盐,可使冰雪快速融化 |
分析 A、根据氢氧化钠固体溶于水时溶液放热,温度明显升高解答;
B、根据硬水的危害判断.
C、根据硝酸铵溶解于水吸收大量的热判断.
D、根据盐水的凝固点比水低判断.
解答 解:
A、氢氧化钠固体溶于水时溶液放热,温度明显升高,故错误;
B、硬水中含有较多可溶的钙、镁化合物,加入洗涤剂产生的泡沫少,去污效果低,所以正确.
C、硝酸铵溶解于水要吸收大量的热,能制得冰袋给高烧病人降温,所以正确.
D、因为盐水的凝固点比水低,冬季向公路上的积雪撒盐,可使冰雪快速融化,所以正确.
故选A.
点评 本题难度不大,掌握常见物质溶于水的吸热与放热现象、温度变化情况是正确解答本题的关键.化学来源于生产、生活,又服务于生产、生活,在学习中要理论联系实际,在实践中理解知识,掌握并运用知识.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:解答题
| 物质 | X | W | Y | Z |
| 反应前质量/g | 10 | 2.2 | 16.2 | 0.9 |
| 反应后质量/g | a | 4.4 | 8.1 | 1.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
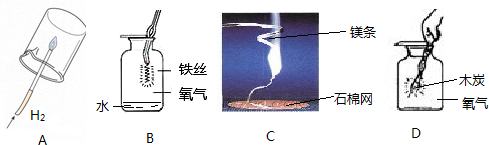
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 不同类别的物质间存在着一定的关系,如图所示.(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质.)碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图所示,回答下列问题:
不同类别的物质间存在着一定的关系,如图所示.(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质.)碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在化学反应前后催化剂的化学性质没有改变 | |
| B. | 催化剂能改变其他物质的化学反应速率 | |
| C. | 在化学反应前后催化剂的质量没有改变 | |
| D. | 在过氧化氢溶液的分解反应中,只能选择二氧化锰作催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
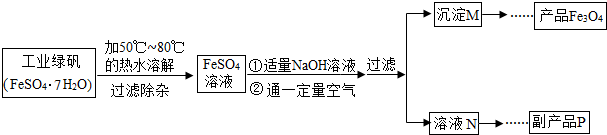
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com