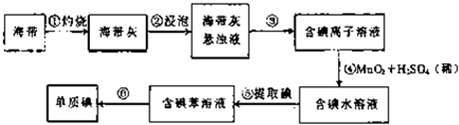
(12分)某研究性学习小组设计并进行了如下实验。
⑴甲组同学用下图装置制取干燥纯净的二氧化碳。请回答下列问题:

①仪器X的名称是 。实验前,关闭活塞,向X中加入水使X中液面高于试管中液面,一段时间后液面保持不变说明 。
②为除去CO2中的HCl气体,B装置中盛放饱和NaHCO3溶液,请写出该反应的化学方程式 。③要得到干燥的CO2,C装置中应盛放 试剂。
④请说明装置B、C中试剂不能交换的原因: 。
⑵乙组同学围绕CO还原CuO产生的红色固体是否一定是Cu进行如下探究:
【查阅资料】①Cu2O粉末呈红色,在酸性溶液中,Cu2O+H2SO4=Cu+ CuSO4+H2O 。②在空气中高温灼烧时:Cu2O稳定,而CuO将分解生成Cu2O和O2。
【提出猜想】猜想Ⅰ:红色固体是Cu;
猜想Ⅱ:红色固体是Cu2O;
猜想Ⅲ:红色固体是 。
【实验探究】步骤Ⅰ:取一定质量的红色固体在空气中高温灼烧,直到质量不再发生改变,称量得到固体的质量增加。说明红色固体中含有 ,写出由Cu生成Cu2O的化学方程式 。
步骤Ⅱ:取一定质量的红色固体投入稀硫酸中,充分反应后溶液呈蓝色。根据以上现象,得到猜想 正确。
【拓展延伸】通过称量红色固体(a g)及灼烧至质量不变时的质量(b g),可以判断红色固体的成分。则欲得到上述实验探究的结果,a、b之间应满足的关系为:128(b-a)/16 a(选填“>”、“<”或“=”)。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案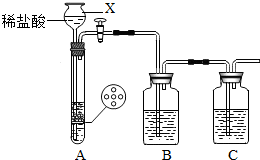 (2012?崇川区一模)某研究性学习小组设计并进行了如下实验.
(2012?崇川区一模)某研究性学习小组设计并进行了如下实验.
 某研究性学习小组设计的实验装置(如图),既可制取气体,又可用于验证物质性质.
某研究性学习小组设计的实验装置(如图),既可制取气体,又可用于验证物质性质.