
| A、化学与健康 | B、化学与能源 |
| ①老年人缺钙会导致骨质疏松 ②人体缺乏维生素A会引起夜盲症 ③要牢记“吸烟有害健康”“毒品万万试不得!” | ①太阳能、核能和天然气都属于新能源 ②电池充电时,化学能转化为电能 ③化石燃料是优质的能源来源,不能作为化工资源 |
| C、物质与分类 | D、化学与环境 |
| ①天然气和海水都属于化合物 ②烧碱和纯碱都属于碱 ③尿素[CO(NH2)2]和硝酸钾(KNO3)都属于复合 肥 | ①施用过量化肥、农药增加粮食产量 ②使用可降解的塑料制品更环保 ③低碳生活,出行尽量步行或骑自行车 |
| A. | A | B. | B | C. | C | D. | D |
分析 本题可以选用排除法是解答,即只要选项中有一项说法错误,即可排除该选项;据此结合化学元素与人体健康的关系、化学与能源、物质的分类、日常生活经验的知识进行分析判断即可.
解答 解:A、老年人缺钙会导致骨质疏松人体缺维生素C会引起坏血病,缺乏维生素A时容易患夜盲症.吸烟有害健康、毒品损害身体,并使人上瘾,万万试不得,故选项归纳正确;
B、天然气是化石燃料,不是新能源,故选项归纳有错误;
C、海水是混合物,纯碱是碳酸钠,不是碱,尿素[CO(NH2)2]是氮肥,不是复合肥,故选项归纳有错误;
D、过量施用化肥、农药不但不会增加粮食产量,还会对土地、环境等造成不良影响,故选项归纳有错误;
故选:A
点评 本题难度不大,但考查的指点较多,本题主要考查了化学元素与人体健康的关系、资源的利用和保护、物质分类、日常生活经验等,选用排除法是正确解答此类题的捷径.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
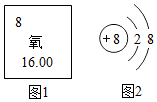 如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.
如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
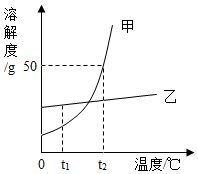 如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:
如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 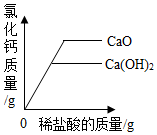 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量 | |
| B. | 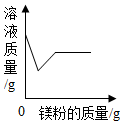 向一定质量氯化亚铁和氯化铝的混合溶液至加入镁粉至过量 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 | |
| D. |  向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
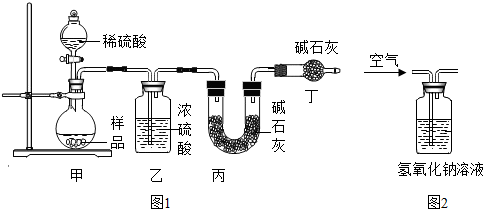

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
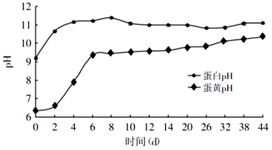 阅读下面科普短文(本文由网络文章改写).
阅读下面科普短文(本文由网络文章改写).查看答案和解析>>
科目:初中化学 来源: 题型:填空题
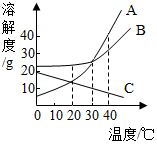 如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.
如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com