
分析 根据硫粉、红磷、木炭燃烧的反应写出反应的化学方程式.
解答 解:硫粉在氧气中燃烧生成了二氧化硫,反应的符号表达式为:S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2;
红磷在空气中燃烧生成了五氧化二磷,反应的符号表达式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
木炭在空气中燃烧生成了二氧化碳,反应的符号表达式为:C+O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2.
故答为:(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(2)S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2;(3)C+O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2.
点评 本题属于基础知识的考查,了解常见物质燃烧的反应是解答本题的基础.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蜡烛在氧气中燃烧,瓶壁有水雾出现 | |
| B. | 铁丝在空气中能剧烈燃烧,火星四射 | |
| C. | 磷燃烧时,会产生大量的白色烟雾 | |
| D. | 硫在空气中燃烧时,会发出蓝紫色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
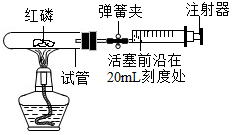 为测定空气中氧气的含量,小华同学打算设计如下方案:选用大试管作反应容器,将过量的红磷放入试管,用橡皮塞塞紧试管口,通过导管与润滑性很好的针筒注射器组成如下图的实验装置.
为测定空气中氧气的含量,小华同学打算设计如下方案:选用大试管作反应容器,将过量的红磷放入试管,用橡皮塞塞紧试管口,通过导管与润滑性很好的针筒注射器组成如下图的实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用10ml量筒取85ml水 | |
| B. | 用常用的PH试纸测得某地水的PH为5.4 | |
| C. | 用托盘天平称得某苏打样品的质量为20.0g | |
| D. | 测得某粗盐中氯化钠的质量分数为98.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 100 | 100 | 100 | 100 |
| 反应生成氢气的质量(g) | 0.2 | 0.2 | 0.2 | 0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com