【答案】
分析:(1)熟练掌握常见的化学仪器名称和用途;
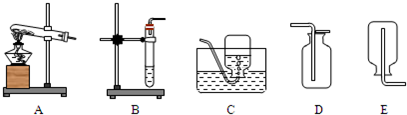
(2)根据反应物的状态和反应条件选择发生装置:固体加热型和固液常温型;根据气体的密度和溶解性选择收集方法;检验CO
2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,看木条是否熄灭;
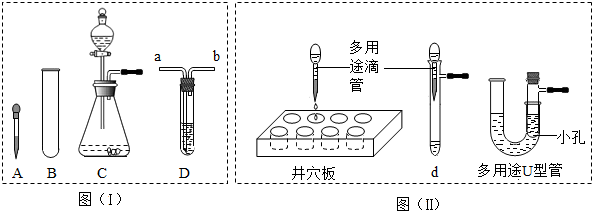
(3)根据发生装置的特点和收集方法选择气体的制取并写出反应的方程式;根据加热高锰酸钾制氧气并用排水法收集时的注意事项进行分析解答;
(4)根据收集一瓶干燥的SO
2,需要干燥装置和合适的收集装置,并选择进气口;
(5)除去氢气中混有的少量水蒸气,可以用浓硫酸干燥;
要验证氢气中是否混有CO
2气体,可以通过澄清的石灰水,看是否变浑浊;
根据氢气的密度比空气小,选择进气管.
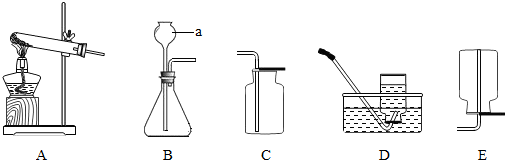
解答:解:(1)a是试管;
(2)制取二氧化碳的药品是石灰石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是B;因为二氧化碳易溶于水,密度比空气大,故收集装置D(向上排空气法);检验CO
2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,若木条熄灭,说明收集满;
(3)该发生装置的特点属于固体加热型,且试管口有一团棉花,因此是加热高锰酸钾制氧气,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;用排水法收集氧气的合适时机是:气泡连续均匀冒出时收集,以防收集的氧气不纯;
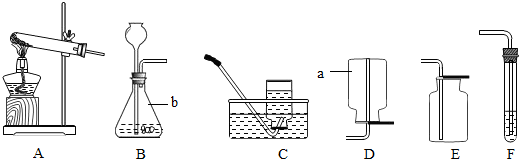
(4)收集一瓶干燥的SO
2,需要浓硫酸干燥,进气管是长进短出;因为密度比空气大,故采用向上排空气法收集,故是长进短出,最后进入尾气处理装置,故连接的顺序为:c→d→b→a;X是浓硫酸;
(5)除去氢气中混有的少量水蒸气,在F瓶内应该盛放的试剂是浓硫酸;
要验证氢气中是否混有CO
2气体,F瓶内应该盛放的试剂是澄清的石灰水;
氧气氢气的密度比空气小,所以进气管是短管,把空气从长管排出进行收集.
故答案为:(1)试管
(2)B、D 将燃着的木条放在集气瓶口,若木条熄灭,则CO
2已收集满
(3)2KMnO
4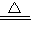
K
2MnO
4+MnO
2+O
2↑ 气泡连续均匀放出
(4)c→d→b→a 浓硫酸
(5)浓硫酸 澄清的石灰水 a.
点评:本题考查了实验室常见气体的制取、收集以及气体的检验、干燥和除杂,综合性比较强.本题型要充分利用题目给出的信息,按照相关知识依次完成.


 K2MnO4+MnO2+O2↑;用排水法收集氧气的合适时机是:气泡连续均匀冒出时收集,以防收集的氧气不纯;
K2MnO4+MnO2+O2↑;用排水法收集氧气的合适时机是:气泡连续均匀冒出时收集,以防收集的氧气不纯;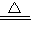 K2MnO4+MnO2+O2↑ 气泡连续均匀放出
K2MnO4+MnO2+O2↑ 气泡连续均匀放出