

分析 (1)根据硫酸铵组成、能提供作物生成所需的元素分析回答;
(2)硫酸铵由溶液中结晶析出的方法是冷却热饱和溶液的方法.据此分析操作过程;
(3)根据制备过程物质的变化关系分析可循环使用的物质;
(4)根据反应物,生成物,反应条件确定化学方程式.
解答 解:(1)硫酸铵能提供作物生成所需的N元素,所以能做氮肥,属于铵态氮肥,它属于盐.
(2)使硫酸铵从溶液中结晶析出的方法是:先加热浓缩形成饱和溶液,再降温冷却,使硫酸铵结晶析出,通过过滤得到硫酸铵晶体,再进行洗涤干燥得到纯净的硫酸铵晶体,所以,正确的操作顺序是②③①④.
(3)由题目信息,碳酸钙高温分解生成了氧化钙和二氧化碳,二氧化碳可以循环使用,所以X是二氧化碳.
(4)用CaSO4、NH3、CO2、H2O制备硫酸铵并生成碳酸钙,反应的化学方程式是:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓.
故答为:(1)氮,盐; (2)②③①④;(3)二氧化碳;(4)CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓.
点评 本题属于新信息题,通过一个陌生的反应考查了有关硫酸铵和二氧化碳的知识,因此同学们要充分利用所给的信息,不要被无用的信息迷惑,结合自己已学过的知识,进行有依据性的判断.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:选择题
| A. | 第一次反应停止时B剩余0.9克 | B. | 第一次反应停止时C剩余0.9克 | ||
| C. | 参加反应A与C的质量比是5:3 | D. | 第二次反应停止时C剩余0.9克 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图所示,向盛水的烧杯中放入一小粒品红,一段时间后,烧杯中形成红色溶液,此实验能说明( )
如图所示,向盛水的烧杯中放入一小粒品红,一段时间后,烧杯中形成红色溶液,此实验能说明( )| A. | 分子处于不断运动之中 | B. | 分子之间有间隔 | ||
| C. | 分子可再分,原子不能再分 | D. | 分子大,原子小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙、丙三种物质的溶解度曲线如图所示.下列叙述正确的是( )| A. | 乙的溶解度最大 | |
| B. | 一定量的溶液由60℃降温至40℃时,乙析出的晶体最多 | |
| C. | 40℃时,乙和丙的饱和溶液中溶质的质量分数相同 | |
| D. | 40℃时,100g水中加入50g丙,所得溶液中溶质的质量分数为33.3% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
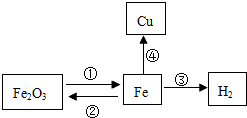 构建知识网络是一种重要的学习方法.如图为某同学绘制的铁的化学性质网络示意图.请分析回答下列问题.
构建知识网络是一种重要的学习方法.如图为某同学绘制的铁的化学性质网络示意图.请分析回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
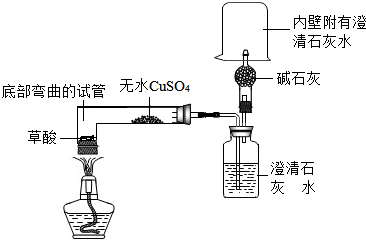 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com