某化学研究性学习小组参加社会社会实践调查得知:某化工厂为综合利用生产过程中的副产品CaSO
4,与相邻的化肥厂联合设计了以下制备(NH
4)
2SO
4的工艺流程.
[工艺流程示意图]
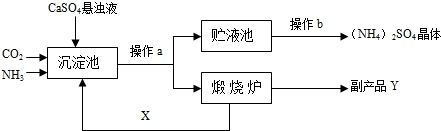
上述流程中,沉淀池中发生的主要化学反应为:CO
2+2NH
3+CaSO
4+H
2O=CaCO
3↓+(NH
4)
2SO
4[讨论交流]
(1)操作a的名称是
,实验室中进行此操作时,用到的玻璃仪器除玻璃棒、烧杯外,还需要
.
(2)经操作a后得到的某物质在煅烧炉中发生反应的化学方程式为
.该工艺中,X在沉淀池中被消耗,在煅烧炉中又生成,故X可循环使用.X的填化学式为
.
(3)图中操作b应怎样进行呢?
查阅资料:右图是硫酸铵在水中的溶解度曲线.
表:固体硫酸铵在部分温度时的溶解度.
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
| 溶解度/g |
70.6 |
73 |
75.4 |
78 |
81 |
85 |
88 |
? |
95 |
98 |
103 |
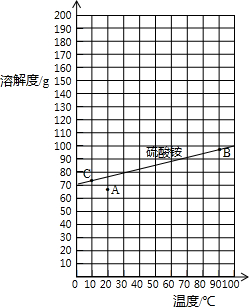
下列说法正确的有
.
①从溶解度曲线中,可以查找70℃时硫酸铵的溶解度约90g;②图中的A点表示硫酸铵溶液的状态不饱和;③若将A点变成B点的操作采用加热蒸发、使溶液浓缩的方法④若将B点转化为C点时,采用的是冷却热饱和溶液方法
该化肥厂生产的硫酸铵化肥品质怎样呢?
[查阅资料]下表是硫酸铵化肥品质的主要指标.
| 指标项目 |
优等品 |
一等品 |
合格品 |
| 外观 |
白色结晶,无可见机械杂质 |
无可见机械杂质 |
| 氮(N)含量 |
≥21.0% |
≥20.7% |
≥20.5% |
氨气极易溶于水,其水溶液为氨水,呈碱性.
已知:(NH
4)
2SO
4+2NaOH
Na
2SO
4+2NH
3↑+2H
2O
[观察外观]该硫酸铵化肥无可见机械杂质.
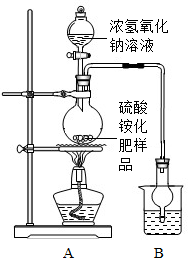
[实验探究]按如图所示装置进行实验.
(1)实验过程中,为使硫酸铵充分反应完全转化为NH
3,则需往烧瓶中加入足量浓氢氧化钠溶液并充分加热.
(2)选择右图装置A进行实验的原因
,烧杯中盛放的试剂稀硫酸可以吸收氨气,两者化合生成一种盐,写出化学方程式
.
[交流讨论]
甲同学认为:应在实验装置中A、B装置间加装一个干燥装置,否则根据实验测得的数据,计算硫酸铵化肥的含氮量可能
(填“偏高”或“偏低”).
乙同学认为:改进后的实验装置中还存在另一个明显缺陷是:
.
(经过大家充分讨论后,对实验装置进行了改进,重新进行实验.)
[探究结论]称取13.5 g硫酸铵化肥样品,用最终改进后的实验装置重新进行实验,经数据处理释放出氨气的质量与反应时间如图所示.试通过计算,判断该化肥的等级.
(要求写出计算过程)






 名校课堂系列答案
名校课堂系列答案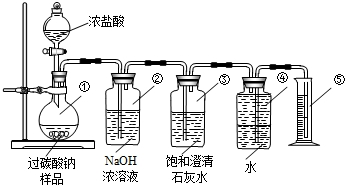
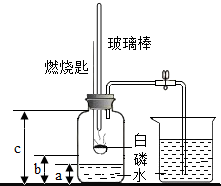 某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.
某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.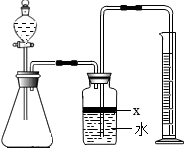 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.