
| A. | 量筒 | B. | 胶头滴管 | C. | 天平 | D. | 玻璃棒 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
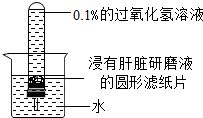 陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的
陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 验证 NaCl 溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在过量的稀硫酸中 |
| D | 比较 Fe、Cu、Al 的金属活动性 | 铁丝浸入 CuSO4 溶液,铜丝浸入 AgNO3 溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
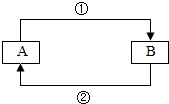 A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.
A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
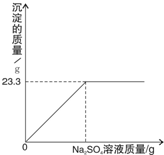 (称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示.试回答下列问题:
(称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
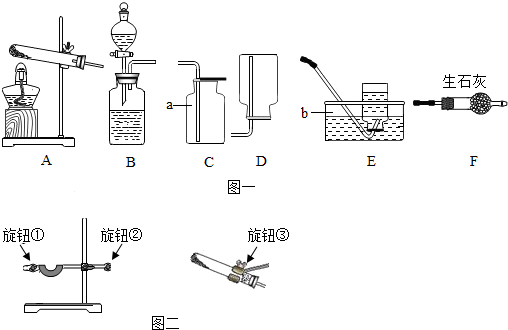
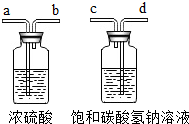
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 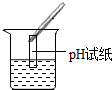 | 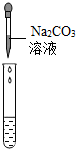 | 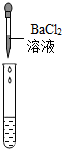 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
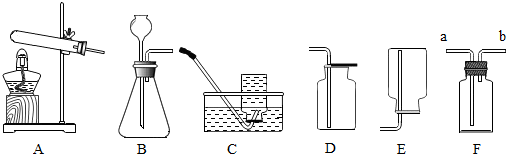
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐 | |
| B. | 在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子 | |
| C. | 某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液 | |
| D. | 将带火星的木条伸入集气瓶中,木条复燃,该气体(氧气)已收集满 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com