
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.据此分析回答有关的问题
解答 解:(1)在金属活动顺序表中,由于铜位于氢的后边,铁位于氢的前边,所以,铜粉中混有少量铁粉,除去铁粉用的药品可以是稀盐酸等;
(2)要比较三种金属的活动性,常采用“三取中”的方法,可以将铜片、锌片分别放入硫酸亚铁的溶液中,铜不能与硫酸亚铁溶液反应,锌能与硫酸亚铁溶液反应,即可得出三种金属的活动性是:锌>铁>铜;
(3)由金属活动性顺序表的应用及题意可知,将X,Y分别放入稀盐酸中,X表面无明显变化,Y表面有气泡产生,说明Y的金属活动性大于X;由将X,Y放入Z的硝酸盐溶液中,X,Y表面均无明显变化,说明金属的活动性是Z大于Y、X,综合以上分析可知,X、Y、Z三种金属的活动性由强到弱的顺序为:Z>Y>X.
故答为:(1)稀盐酸;(2)铜片、锌片分别放入硫酸亚铁的溶液中,铜不能与硫酸亚铁溶液反应,锌能与硫酸亚铁溶液反应,即可得出三种金属的活动性是:锌>铁>铜;(3)Z>Y>X.
点评 利用金属活动性顺序,可知金属的活动性;学会利用它们处理和解释问题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室制取气体时,先检查装置气密性,再装药品 | |
| B. | 检查装置气密性时,先用手握住试管,后将导管伸入水中 | |
| C. | 稀释浓硫酸时,先在烧杯内倒入水,再缓慢注入浓硫酸,并不断搅拌 | |
| D. | 用排水法收集氧气,当气体收集满时,先把导管移出水面再熄灭酒精灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 铁画边角料 | 稀硫酸 | 剩余固体和液体的总质量 |
| 8.5 | 170 | 178.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | 氧化铜粉 | 炭粉 | 在空气中充分灼烧 |
| C | 氯化钙溶液 | 盐酸 | 加过量碳酸钙,过滤 |
| D | FeSO4溶液 | CuSO4溶液 | 加入足量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
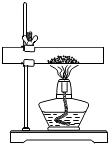 广东省韶关市盛产石灰石,某校课外兴趣小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析.
广东省韶关市盛产石灰石,某校课外兴趣小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com