
【题目】工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。
![]()
⑴氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显________色。
⑵从步骤①提取粗盐常用___________(填“蒸发结晶”或“降温结晶”)方法。
⑶从酸碱反应的角度分析,步骤④中通入氨气的作用是____________________。
⑷步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途______。
⑸步骤⑥中发生反应的化学方程式为______________,该反应类型属于________反应。
⑹工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
时间/s | 0 | 5 | 10 | 15 |
读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
请你据此分析计算:
①实验中产生二氧化碳的质量为____________;
②该产品中碳酸钠的质量分数_______(写出计算过程,结果精确到0.1%)
【答案】 红色 蒸发结晶 氨气溶于水形成碱性溶液,有利于吸收二氧化碳 治疗胃酸分泌过多(其它合理也可) 2NaHCO3 △ Na2CO3+H2O+CO2↑ 分解 6.6g ②96.4%
【解析】⑴氨碱法生产所得产品为纯碱,即碳酸钠,其溶液呈碱性,所以向纯碱水溶液中滴入无色酚酞试液显红色。⑵从步骤①提取粗盐常用蒸发结晶方法。因为氯化钠的溶解度受温度的影响较小,改变温度不利于氯化钠结晶析出。⑶从酸碱反应的角度分析,步骤④中通入氨气的作用是生成氨水,使溶液呈碱性,有利于二氧化碳的吸收。⑷碳酸氢钠在生产和生活中有许多重要用途,如:灭火剂的主要成分,发酵粉的主要成分,治疗胃酸过多等。⑸碳酸氢钠在加热条件下分解生成碳酸钠、二氧化碳、水,发生反应的化学方程式为2NaHCO3 △ Na2CO3+H2O+CO2↑,该反应类型属于由一种物质生成两种或两种以上的物质的反应叫分解反应。⑹由质量守恒定律可知反应前后物质的总质量不变,所以二氧化碳的质量为:215.2g-208.6g=6.6g,设 产品中碳酸钠的质量为x,则Na2CO3+2HCl====2NaCl+H20+CO2↑
106 44
x 6.6g
106/x=44/6.6g
x=15.9g
产品中碳酸钠的质量分数=15.9g÷16.5g×100%=96.4%
答:略


 高中必刷题系列答案
高中必刷题系列答案科目:初中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法错误的是
A. 用灼烧的方法可以区分蚕丝和棉纱
B. 食用油反复加热会产生大量有害物质
C. 加热能杀死流感病毒是因为蛋白质受热变性
D. 医用消毒酒精中乙醇的体积分数为95%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列数据合理的是
A.用托盘天平称取12.62g的食盐
B.用10mL量筒量取8.76mL蒸馏水
C.普通温度计显示的室温读数为25.68℃
D.用10mL量筒量取某溶液体积为8.2mL
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是
A.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C.在两瓶相同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
D.在两瓶不同浓度的氧气中,分别同时进行相同铁丝的燃烧实验
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正确的是
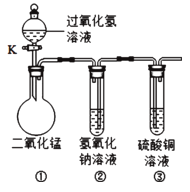
A. 打开活塞K,装置①中会有气泡冒出,黑色固体消失
B. 打开活塞K,装置②中会看到液面上升,产生蓝色沉淀
C. 打开活塞K,装置②中会有气泡冒出
D. 打开活塞K,装置③中会有液体流入,产生蓝色沉淀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据报道:某地一名5岁的女孩子把涂改液当饮料吸食,食道被严重烧伤。经医院检测后发现,涂改液中含有苯、甲基环已烷等多种有毒物质。由此可知,涂改液是
A.混合物 B.纯净物 C.单质 D.化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是
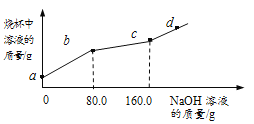
A. ab段反应产生蓝色沉淀
B. bc段溶液增加70.2g
C. c点对应的溶质质量分数为4.9%
D. d点溶液中溶质有2中,且PH>7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末,可能是FeCl3、CaCO3、BaCl2、Na2SO4、KOH、KNO3中的一种或几种,为证明其组成,进行如下实验:

根据上述实验现象判断:
①白色固体中一定不含____________,一定含有______________,可能含有____________
②上述过程中通入CO2产生白色沉淀的化学式是_______________。
③写出滴加稀盐酸白色沉淀全部溶解的化学方程式______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】60 ℃时,将36 gKNO3溶于204 g水中,全部溶解后,溶液中溶质的质量分数为________。将此溶液均分成三等份:
(1)取第一份溶液,将温度升至100 ℃,所得溶液中溶质的质量分数为________;
(2)取第二份溶液,将其质量分数变为原来的两倍,需加入固体_________ g;
(3)取第三份溶液,使其溶质的质量分数变为原来的一半,需加水________ g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com