
已知CaCl2和Na2CO3能发生复分解反应,下列所示的图象能反映相对应实验的是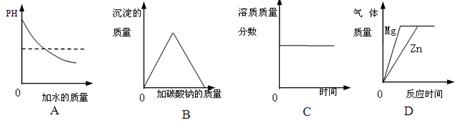
| A.常温下向pH=13的NaOH溶液中不断加水稀释 |
| B.向盐酸和氯化钙的混合溶液中加入碳酸钠 |
| C.将60℃饱和的硝酸钾溶液加热蒸发水分至有白色晶体析出 |
| D.将足量的金属镁片和锌片分别和等质量、相同质量分数的稀硫酸混合 |
D
解析试题分析:根据具体变化时的物质量的关系,结合图像分析判断。
A、氢氧化钠溶液加水稀释碱性减弱,pH随之变小,但pH不可能小于7,错误;
B、向盐酸和氯化钙的混合溶液中加入碳酸钠,盐酸和氯化钙都能与碳酸钠反应,分别生成气体和沉淀,但生成的沉淀会与盐酸反应,故开始时无沉淀出现,错误;
C、若恒温蒸发饱和硝酸钾溶液,随着溶剂的蒸发,会有溶质析出,故溶液始终是该温度下的饱和溶液,则溶质质量分数保持不变;但若升高温度蒸发水分,由于硝酸钾的溶解度随温度的升高而增大,故开始蒸发水分时,应无晶体析出,则溶质质量分数会增大,错误;
D、足量的镁和锌分别与硫酸反应时,生成的氢气质量相等,并且因为镁比锌活泼,所以反应的速率快,正确。故选D
考点:复分解反应及其应用
点评:本题是化学反应中定量关系和图象相结合的题型,题目难度较大;要准确解答此类题,关键要对化学反应知识熟练,并能结合图象的数学意义,综合考虑;图象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程。


科目:初中化学 来源: 题型:
 27、实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是
27、实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 适量的稀盐酸 |
产生大量的气泡 | 该溶液是 该溶液是碳酸钠溶液 相关的化学方程式 Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 稀盐酸(或稀硫酸) 稀盐酸(或稀硫酸) |
产生大量的气泡 | 该溶液是 碳酸钠溶液 碳酸钠溶液 ,反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2013?如东县模拟)实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
(2013?如东县模拟)实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 步骤一:取样品于试管中,滴加足量 稀盐酸 稀盐酸 |
产生大量的气泡 | 猜想①正确. 步骤一发生反应的化学方程式是 Na2CO3+2HCl═2NaCl+CO2↑+H2O Na2CO3+2HCl═2NaCl+CO2↑+H2O |
| 步骤二:把产生的气体,通入 澄清石灰水 澄清石灰水 |
石灰水变浑浊 石灰水变浑浊 |
| 探究步骤 | 预计现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的 CaCl2(或BaCl2等) CaCl2(或BaCl2等) 溶液并过滤 |
产生白色沉淀 | 溶液中: 既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变 红 红 色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com