
【题目】用化学用语填空
(1)3个硫原子_____;
(2)4个铵根离子_____;
(3)碘酒中的溶剂_____;
(4)熟石灰_____。
 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:
【题目】加热氯酸钾(化学式为KClO3)和催化剂二氧化锰的混合物可制备氧气,同时生成氯化钾,该反应的化学方程式为________,但实验中发现有刺激性气味的气体产生。
【提出问题】刺激性气味的气体是什么呢?
【猜想假设】猜想一:臭氧(化学式为O3) 猜想二:HCl 猜想三:Cl2
同学们认为不需实验验证就可以判断猜想________是错误的,理由为________。
【查阅资料】
(1)C12+H20===HC10+HCl, AgNO3 +HCl===AgCl↓ + HNO3。
(2)臭氧在MnO2存在的情况下极易分解成氧气。
(3)氯气可使湿润的淀粉碘化钾试纸变蓝。
【实验探究】
查阅资料后大家认为猜想一是错误的,理由为________。
他们进一步又做了如下实验:取氯酸钾和二氧化锰的混合物放人试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管口(如右图),看到的现象是________,再将湿润的淀粉碘化钾试纸悬于试管口,试纸变________色,最终证明猜想三正确。
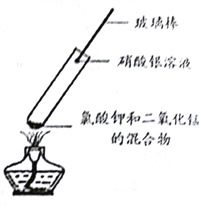
【反思拓展】
(1)欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的________在反应前后不变。
(2)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Clˉ和ClOˉ,而野外常用漂白粉[主要成分化学式为Ca(ClO)2]。你认为在水中起杀菌消毒作用的离子是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下面的装置和仪器用品图示回答问题:
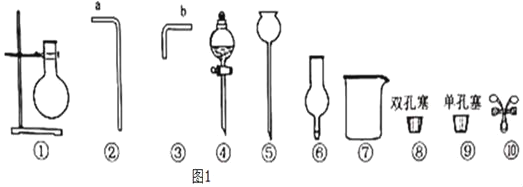
(1)仪器⑤的名称是_____。
(2)实验室用大理石与酸反应制取二氧化碳时,可用⑥、⑦和_____组装成能控制反应发生和停止的发生装置,⑥中装入的大理石须是_____(填“粉状”或“块状”)的,⑦中装入的酸通常是_____(写名称)。
(3)实验室用双氧水和二氧化锰制取氧气的化学方程式为_____。若要达到控制该反应速率的目的,可用图中的_____(填序号)组装成发生装置。若选择①②③⑧组装成排空气收集氧气的装置,则氧气应从_____(填“a”或“b”)口通入。
(4)小明同学利用(3)制得的氧气并设计下列装置来测定一种氧化铜和炭粉的混合物中碳的质量分数,请回答相关问题:
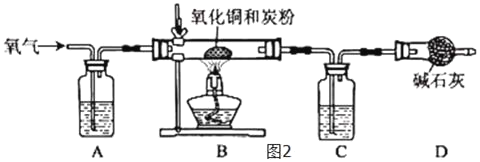
①仪器组装好后要检查装置的_____。
②A、C两瓶中所装试剂依次为_____、_____(选填序号)
I.碳酸氢钠溶液Ⅱ.浓NaOH溶液Ⅲ.浓硫酸
③小明设计装置D的意图是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是( )

A. 反应前后各元素化合价不变
B. 参加反应的CO2和H2分子个数比为1:3
C. 该反应不符合质量守恒定律
D. 该化学变化中发生改变的微粒是原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二十一世纪是海洋开发与利用的世纪,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:下图是利用海水提取粗盐的过程。

海水晒盐是________________ (填“物理”或“化学”)变化,上图中①是___________(填“蒸发”或“冷却”)。
(2)粗盐提纯:粗盐中含有少量CaCl2、MgCl2、Na2SO4和泥沙,某同学将该粗盐进行提纯。
①将粗盐加适量水溶解,然后进行________________,除去泥沙等难溶性杂质,得到澄清溶液;
②向所得的澄清溶液中依次加入稍过量的BaC12溶液、NaOH溶液和________________(用化学式表示)溶液,除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯净的NaCl溶液。
③蒸发溶液,当________________时停止加热,他注意到不能立即把直接放在实验台上,以免烫坏实验台。
(3)氯碱工业基本流程:

由图示可知,该工艺中可循环利用的物质是________________。
(4)海水制镁流程:

写出步骤①中生成Mg (OH)2的反应的化学方程式________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某农场附近新建了一座燃煤火力发电厂后,该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的pH如下表:
作物 | ① 水稻 | ② 小麦 | ③ 玉米 | ④ 油菜 | ⑤ 马铃薯 |
pH | 6~7 | 6.3~ 7.5 | 6~ 7 | 6~ 7 | 4.8~ 5.5 |
(1)根据上表数据,你认为这种土壤最适合种植的作物是_________ (填编号)
(2)若继续种小麦,你认为最好选用以下__________(填编号)试剂来改良土壤.
①工业盐酸 ②熟石灰 ③纯碱 ④烧碱
(3)该地区形成酸雨的过程用化学方程式可简单表示为_________。
(4)可以用氨水处理该厂排放的废水中含有的硫酸,反应的化学方程式为_____。
(5)2017年5月18日,中国首次可燃冰试采成功,这标志着我国可燃冰开采技术已居世界前列.可燃冰的化学式为CH4·8H2O ,其外观像冰一样但遇火即可燃烧.
①可燃冰属于______(填“可”或“不可”)再生资源.为缓解能源危机,人们还必须积极开发利用新能源,请写出一种新能源___________;
②取一定质量的CH4和25.6gO2在密闭容器中点燃;恰好完全反应,生成agCO、bgCO2和18gH2O ,则a+b=___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图A、B、C、D、E、F是初中常见的六种物质,且都含有一种相同的元素,A和C是两种酸,E 可以制肥皂,用“一”表示两种物质间能发生化学反应,“→”表示一种物质可以通过一步反应转化为另一种物质,(部分反应物和生成物及反应条件已略去)。
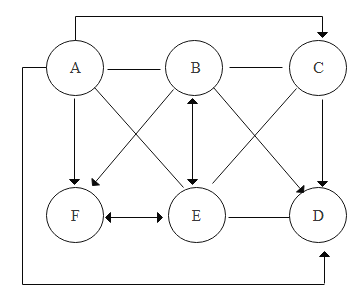
(1)请写出化学式C:_____D:_____。
(2)写出E转化F的方程式_____。
(3)A溶液与B溶液反应的实验现象_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组用干电池、生石灰等仪器和试剂进行电解水的实验改进与探究。
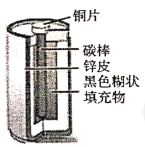
实验一:探究干电池构造:酸性锌锰干电池内部结构如图所示,小组同学取出铜片、碳棒、锌皮和黑色糊状填充物。并查阅资料知道了其中的黑色糊状填充物由炭黑、MnO2、ZnCl2和另一种氯化物等组成。
(1)将黑色糊状填充物溶于水, __________________(填操作名称)得到溶液和固体,用石蕊试纸检验溶液呈红色,表明溶液呈__________________性。
(2)在溶液中加入生石灰,能闻到强烈的氨味,生石灰与水反应的化学方程式为__________________,黑色糊状填充物中另一种氯化物的化学式为__________________。
(3)从得到的固体中得到较纯的MnO2,可采用的简便方法是__________________。
(4)将6.5g锌皮与足量稀盐酸完全反应,则生成氢气的质量大于0.2g,由此推测锌皮还可能含的另外一种金属是______________。 (填答案字母序号)
a 锡
b 铁
c 铅
实验二:电解水的实验改进用电池中取出的碳棒作电极,用生石灰制成的Ca(OH)2饱和溶液增强水的导电性,进行电解水的实验。实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
[猜想与假设]
①溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②水减少导致Ca(OH)2析出而出现白色浑浊。
③与碳棒电极材料有关。
[实验操作]
实验 | 实验装置 | 主要实验操作 | 实验现象 |
1 | 取20mLCa(OH)2饱和溶液加热至沸腾 | 溶液中未出现白色浑浊 | |
2 |
| 用碳棒为电极,取饱和溶液于烧杯中,加5mL水,通电3分钟 | 烧杯中溶液体积几乎无明显变化,溶液中明显出现白色浑浊 |
3 | 改用铜片为电极,另取饱和溶液于烧杯中,加5ml水通电3分钟 | 与电源正极相连的铜电极变黑, 溶液中未出现白色浑浊 |
[解释与结论]
(5)实验1得出的结论是_______________________。
(6)猜想与假设②不成立,依据的现象是______________________。
(7)实验3中铜电极上的黑色物质是_______________________,要除去该物质需要的试剂是__________________。(填化学式)
[结论与反思]
(8)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是______________________。(用化学方程式表示)
(9)实验3中更换石墨电极为铜电极的目的是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com