




科目:初中化学 来源:不详 题型:实验题

| | 样品 质量 | 装置及药品 总质量 | 装置及反应后物质 总质量 |
| 实验数据 | 144g | 394g | 378g |

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

 NH3↑+HCl↑
NH3↑+HCl↑ | 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.取少量溶液样品,滴入氯化钡溶液,有白色沉淀生成 |
| B.取一定量溶液样品,滴入稀盐酸,立即有大量气体产生 |
| C.取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中不一定含有氢氧化钠 |
| D.向溶液样品中加入适量的澄清石灰水至恰好完全反应,过滤,可除去样品中的杂质 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论 |
| | | 该漂白液已完全失效 |
| 实验操作及实验现象 | 实验结论 |
| 取少量该漂白液于试管中,加入过量的稀盐酸。观察到 | 猜想①不合理 |
| | 猜想③不合理,②合理 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
 (1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
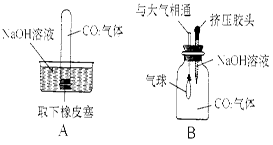
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com