
| A. | 10g/100g水 | B. | 20g/100g水 | C. | 25g/100g水 | D. | 无法计算 |
 走进文言文系列答案
走进文言文系列答案科目:初中化学 来源: 题型:填空题
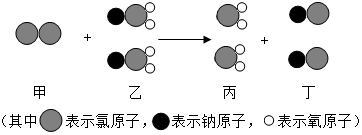 ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题:
ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜想 | 实验操作 | 现象和结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
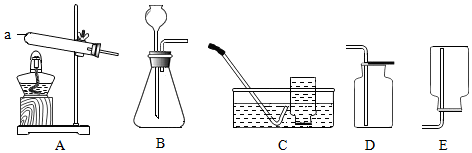
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
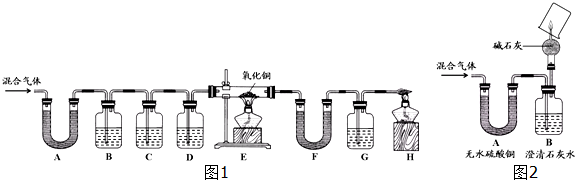
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 方案一:加锌粒 | 方案二:滴加酚酞溶液 |
| 实验操作 | 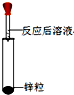 |  |
| 实验现象 | ⑤产生气泡 | 无明显现象 |
| 实验结论 | 溶液中有HCl | 溶液中无⑥Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
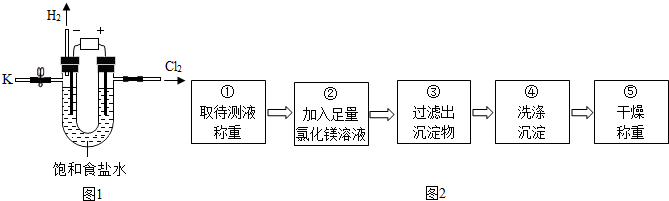
| 实验步骤 | 实验现象 | 实验结论 |
| 待测液中含有氢氧化钠. |
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH>H2SO4>NaCl | B. | NaOH>NaCl>H2SO4 | C. | H2SO4>NaCl>NaOH | D. | H2SO4>NaOH>NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com