
【题目】小芳对复分解反应发生的条件产生兴趣,于是她和小组内同学仅用以下药品展开了探究。
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、氯化钠溶液、酚酞试液
(提出问题)复分解反应发生的条件是什么?
(查阅资料)硝酸钡溶液显中性,且Ba2+有毒。
(实验探究)小芳用上述物质做了下列几组实验
组合序号 | (1) | (2) | (3) | (4) | (5) | (6) |
组合物质 | 稀盐酸 氯化钠 | 稀盐酸 氢氧化钠 | 稀盐酸 碳酸钠 | 稀硫酸 硝酸钡 | 氯化钠 硝酸钡 | 硝酸钡 碳酸钠 |
(记录和解释)
(1)组合(1)、(2)、(5)均无明显现象,其中组合___________与另外两组的实质不同。为证明该不同之处,小芳在实验过程中使用了酚酞试液。
(2)请写出组合(6)的化学方程式___________。
(实验结论)他们通过实验探究并请教老师后知道,只有当两种化合物互相交换成分,生成物中有___________生成时,复分解反应才可以发生。
(拓展延伸)实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。为了确定沉淀和清液的成分,继续展开探究。
(实验1)探究沉淀的成分。
(提出猜想)I.沉淀只有硫酸钡 II.___________, III.沉淀中含有硫酸钡和碳酸钡
小莲取少量沉淀于试管中,滴加过量的___________(请补充完整实验操作和观察到的现象),证明了猜想III是正确的。
(实验2)探究清液的成分。
①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。
②另取少量清液于另一只试管中,滴加___________,有白色沉淀产生。
(解释与结论)探究活动结束后,小组内成员通过讨论分析,一致认为清液中一定没有的离子是___________(指示剂除外,且不考虑水的电离)。
(处理废液)为了防止污染环境,小芳对废液进行处理,将固体回收进一步处理,溶液排放。
(交流与反思)根据你对复分解反应发生条件的了解,请写出一个题中实验药品间除(1)~(6)组合之外,能发生复分解反应的化学方程式___________。
【答案】(2) ![]() 沉淀或气体或水 沉淀只有碳酸钡 稀盐酸,沉淀部分溶解,有气泡产生 稀硫酸(或Na2CO3溶液); OH-、CO32-、 SO42-、H+
沉淀或气体或水 沉淀只有碳酸钡 稀盐酸,沉淀部分溶解,有气泡产生 稀硫酸(或Na2CO3溶液); OH-、CO32-、 SO42-、H+ ![]()
【解析】
记录和解释:(1)稀盐酸和氯化钠不反应,因此无明显现象,稀盐酸和氢氧化钠反应生成氯化钠和水,无明显现象,氯化钠和硝酸钡不反应,无明显现象,故(1)、(5)是因为没有反应。而无明显现象,(2)发生了反应,故与另外两组的实质不同的是(2)
(2)硝酸钡与碳酸钠反应生成碳酸钡和硝酸钠,该反应的化学方程式为:![]() ;
;
实验结论:复分解反应的条件是:只有当两种化合物互相交换成分,生成物中有沉淀、气体、水生成时,复分解反应才可以发生;
实验1:
提出猜想:将所有废液收集在废液缸中静置,出现白色沉淀,这些物质中,只有硝酸钡能与碳酸钠反应生成碳酸钡沉淀,硝酸钡和硫酸反应生成硫酸钡沉淀,故白色沉淀可能是碳酸钡,也可能是硫酸钡,也可能是碳酸钡和硫酸钡的混合物,故Ⅱ、沉淀只有碳酸钡;
结论为猜想III是正确的,故沉淀为碳酸钡和硫酸钡的混合物,碳酸钡能与稀盐酸反应生成氯化钡、二氧化碳和水,硫酸钡与稀盐酸不反应,故可滴加过量稀盐酸,沉淀部分溶解,有气泡产生,说明含碳酸钡和硫酸钡;
实验2:
②有沉淀产生,由以上分析可知,废液中只能产生硫酸钡、碳酸钡沉淀,有沉淀产生,说明清液中含钡离子,故可加入稀硫酸或碳酸钠;
解释与结论:①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。钡离子能与硫酸根离子结合成硫酸钡沉淀,也能与碳酸根离子结合生成碳酸钡沉淀,故无明显现象,说明溶液中不含硫酸根离子和碳酸根离子;
由②可知,含有钡离子;
将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液,无色上层清液,说明不含氢氧根离子,因为无色酚酞遇碱变红,由以上分析可知,白色沉淀中含碳酸钡,故上层清液中不含氢离子,因为氢离子能与碳酸钡反应,不能共存。
故清液中一定没有的离子是:OH-、CO32-、 SO42-、H+;
交流反思:由所给试剂可以看出,稀硫酸也能与氢氧化钠反应生成硫酸钠和水,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应,该反应的化学方程式为:![]() 。
。


科目:初中化学 来源: 题型:
【题目】某氢氧化钠样品中可能混有Na2SO4和Na2CO3杂质,化学实验小组的同学们为了探究该氢氧化钠样品中杂质的成分,并提纯样品,做了如下探究实验:取少 量氢氧化钠样品,加足量水溶解,待用。
(实验探究1)甲同学:如图所示,取一定量氢氧化钠样品溶液于试管中,向其中加入稀硫酸,观察到溶液中有气泡冒出,再向其中滴加硝酸钡溶液,观察到溶液中有白色沉淀产生
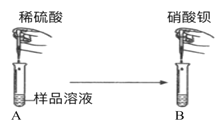
(1)请你写出该过程中,最先发生的化学反应的方程式:___________;
(2)根据实验现象,甲同学得出结论:样品中含有的杂质为碳酸钠和硫酸钠。 请你评价甲同学的实验结论:________。
(提出问题)将B试管中混合物过滤,测得滤液pH>7,则所得滤液中含有哪些离子?
猜想一:Na+、NO3-、OH-、Ba2+
猜想二:Na+、NO3-、OH-、SO42-
猜想三:Na+、NO3-、CO32-
(3)你的猜想是:________ (填离子符号)
(4)上述猜想中一定错误的是________。
(实验探究2)乙同学:另取少量氢氧化钠样品溶液于试管中,向其中先加入________,再加入硝酸钡溶液,观察到_________,则证明样品中含有两种杂质。
(表达与交流)同学们经过讨论后认为,要除去氢氧化钠样品中的杂质,只需要向样品的溶液中加入一种试剂,即_________溶液,充分搅拌后过滤,蒸发结晶即可得到纯净的氢氧化钠固体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组的同学利用下列装置,用高锰酸钾制取氧气,并完成细铁丝燃烧实验。
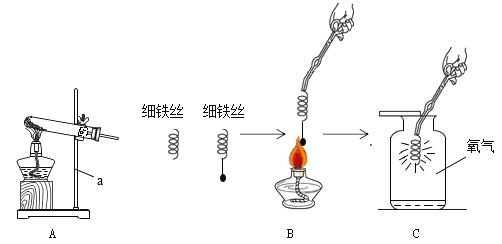
(1)仪器a的名称_____。
(2)高锰酸钾制取氧气的化学反应方程式为_____,试管口放一团棉花的目的是_____。
(3)铁丝在空气中不能燃烧的原因是_____。 铁丝下端系一根火柴的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为了研究影响分子运动速率的因素,利用浓氨水挥发出来的氨气和浓盐酸挥发出来的氯化氢气体发生反应生成白色氯化铵固体的原理,设计了如图所示的实验。实验开始时,两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,一段时间后,先在A处产生大量白烟,然后白烟逐渐充满整个玻璃管。
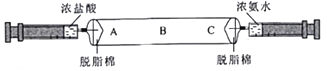
回答下列问题:
(1)写出实验中反应的化学方程式______。
(2)此实验证明:相对分子质量越大,分子的运动速率越______![]() 填“大”或“小”
填“大”或“小”![]() 。
。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是
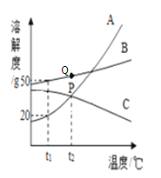
A.t2℃时,A、C两种溶液中溶质的质量相等
B.t1℃时,100g B物质的饱和溶液中溶质的质量是50g
C.要将B溶液的状态由Q点转化为P点,可以加适量溶剂
D.分别将t2℃时B、C两种物质的饱和溶液降温至t1℃,均有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表.下列说法错误的是( )
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 2 | 20 | 14 | 2 |
反应后质量/g | m | 28 | 0 | 8 |
A.m的值是2B.甲可能是该反应的催化剂
C.反应的乙、丁质量比是4:3D.该反应是化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读资料并结合身边实际回答问题。
84消毒液等物资在学校防疫工作中扮演了重要角色。次氯酸钠(NaClO)是84消毒液的有效成分,其水溶液呈碱性,能缓慢分解,受热或光照会快速分解;其强氧化性可用于水的净化、造纸、纺织品(如布匹、毛巾、汗衫等)漂白、制药、精细化工、卫生消毒等众多领域。
次氯酸钠反应产生的次氯酸易挥发、具有强氧化性,可导致蛋白质变性,实现消毒。浓度大的情况下会对人体呼吸道产生损伤,对金属有腐蚀作用。
(1)84消毒液是_____(填“纯净物”或“混合物”)。
(2)教室喷洒的消毒液是用84消毒原液和水按照体积比1:200配置的,则20升水需要_____mL84消毒原液。
(3)下列关于防治新冠疫情的做法正确的是_____(多项选择)
A 每天教室喷洒消毒液的次数越多越好
B 个人勤洗手、教室多通风
C 喷洒过消毒液的教室在同学返回前应该先通风
D 每天应该定期用75%的酒精擦拭楼梯扶手等公共设施
(4)学校防疫物资储备室通常要用窗帘遮光,这样做的目的是什么_____?
(5)我们通常认为大家在教室逗留的时间长,所以校园里教室的消毒比其他地方更重要,但是室外消毒液浓度却比室内消毒液浓度大。请解释为什么室外消毒液浓度大_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com