
【题目】电石是一种重要的化工原料。同学们借助网络资源和化学实验对电石的性质和变化进行科学探究。
(查阅资料)①电石的主要成分为碳化钙。
②CaC2与水反应,生成一种白色固体和一种可燃性气体。
(提出猜想)根据碳化钙及水的组成推测:
①碳化钙与水反应生成的白色固体可能是___或碳酸钙。
②碳化钙与水反应生成的可燃性气体可能是H2、CH4或C2H2(乙炔)。
(实验探究)同学们在老师的指导下,按如下步骤进行实验:
①取适量的电石加水,收集反应生成的气体,验纯后点燃,发现气体燃烧时产生黄色火焰并伴有浓烈黑烟,因此,该气体不可能是____。
②取反应生成的白色固体分装于两支试管里,向一支试管里滴加足量的稀盐酸,固体溶解,但没有产生气体,说明白色固体是__。
(问题交流)①存放电石的库房若发生火灾,___(填“能”或“不能”)用水扑救。
②保存和运输电石时,必须防___和防____。
③实验室常用电石与水反应制取乙炔(难溶于水),写出有关反应的化学方程式:___,选用的发生装与收集装置的组合是如图中的___(填装置编号)。
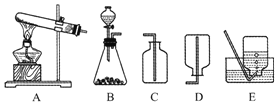
【答案】氢氧化钙 氢气 氢氧化钙 不能 水 潮 CaC2+2H2O═Ca(OH)2+C2H2↑ BE
【解析】
[提出猜想]由质量守恒定律可知,碳化钙与水反应生成的白色固体可能是氢氧化钙或碳酸钙;故填:氢氧化钙;
[实验探究]①氢气燃烧产生淡蓝色火焰,而该气体燃烧时产生黄色火焰并伴有浓烈黑烟,因此,该气体不可能是氢气;故填:氢气;
②氢氧化钙与盐酸反应生成氯化钙和水,而碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,取反应生成的白色固体分装于两支试管里,向一支试管里滴加足量的稀盐酸,固体溶解,但没有产生气体,说明白色固体是氢氧化钙而不是碳酸钙;故填:氢氧化钙;
[问题交流]①因为电石能与水反应生成可燃性气体,所以存放电石的库房若发生火灾,不能用水扑救;故填:不能;
②由于电石能与水反应,因此保存和运输电石时,必须防水、防潮;故填:水;潮;
③实验室制取乙炔的化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑.实验室制取乙炔不需要加热,应该用B装置作为发生装置;因为乙炔密度比空气略小,不能用排空气法收集,乙炔不溶于水,可以用排水法收集,即用E装置收集;故填:CaC2+2H2O═Ca(OH)2+C2H2↑;BE。


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:初中化学 来源: 题型:
【题目】化学概念在逻辑上可能存在如图所示关系,对下列概念说法正确的是( )
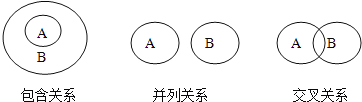
A. 纯净物与混合物属于包含关系
B. 化合物与氧化物属于并列关系
C. 单质与化合物属于交叉关系
D. 化合反应与分解反应属于并列关系
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)我省两淮地区煤炭资源丰富,瓦斯存在于煤层及周围岩层中,是井下有害气体的总称,主要成分是甲烷。
(1)请你写出甲烷完全燃烧的化学方程式:__________________________________。
(2)煤矿瓦斯爆炸有两个必要条件:
①瓦斯含量在爆炸极限的范围内;②________________________________________。
(3)下表是常见三种气体的爆炸极限,请你据此判断:
最容易发生爆炸的气体是____。
可燃气体 | 爆炸极限(体积分数) |
H2 | 4.0%~74.2% |
CH4 | 5%~15% |
CO | 12.5%~74.2% |
(4)下列图标中,与燃烧和爆炸无关的是
![]()
A B C D
(5)某现代化的矿井采用了“低浓度瓦斯发电技术”,有效解决了矿区及周边地区的照明用电。这种既采煤又发电联合生产的优点是___________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O42H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成,探究过程如下:
(查阅资料)
①硫酸铜晶体(CuSO45H2O)受热时会发生如下反应: CuSO45H2O![]() CuSO4+5H2O草酸亚铁晶体(FeC2O42H2O)也能发生类似的反应;
CuSO4+5H2O草酸亚铁晶体(FeC2O42H2O)也能发生类似的反应;
②草酸亚铁晶体热分解的气体产物是H2O,CO,CO2;
③白色的无水CuSO4遇水蒸气会变成蓝色;
④浓硫酸具有吸水性,是常用的气体干燥剂;
⑤浓的氢氧化钠溶液易吸收大量的二氧化碳气体,比石灰水吸收效果好。
(实验设计)
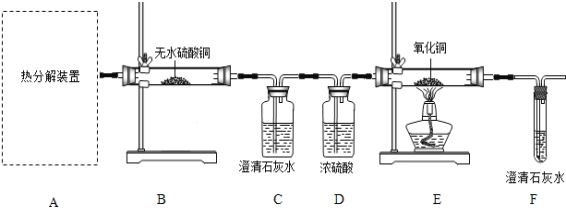
(1)从环保角度考虑,该套实验装置的明显缺陷是_______。
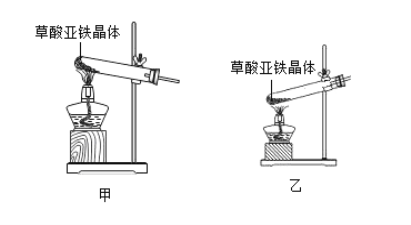
(2)可选择以下实验装置中的_____(选填“甲”或“乙”)作为虚线中的“热分解装置”。
(问题讨论)
(3)实验过程中如果观察到以下现象:B中白色无水CuSO4变成蓝色,___________,E中黑色粉末变成红色,则可证明草酸亚铁晶体热分解的气体产物是H2O,CO,CO2;写出F装置中所发生反应的化学方程式_________。
(4)该兴趣小组进行上述实验时,应先点燃__________处(填“A”或“E”)的酒精灯,原因是____________。
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需对实验设计方案进行改进,请说出你的改进措施________。
(数据分析)
(6)称取3.60g草酸亚铁晶体(FeC2O42H2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:
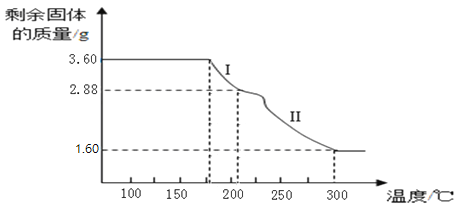
①过程Ⅰ发生反应的化学方程式为____________。
②已知:300℃时草酸亚铁晶体完全分解后剩余固体只有一种且是铁的氧化物。通过计算可确定该氧化物为_____________(填名称)。(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是( )
图象 |
|
|
|
|
变化关系 | 高温煅烧石灰石 | 向一定量镁条中加入过量稀盐酸 | 向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水 | 加热一定量的高锰酸钾 |
选项 | A | B | C | D |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,已知![]() 的化学式为HClO,是一种酸。
的化学式为HClO,是一种酸。
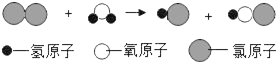
(1)该反应前后化合价没有发生变化的元素符号为_____;
(2)该反应中参加反应的单质与氧化物的质量比为_____;
(3)上述反应发生后加人NaOH溶液,发生反应的化学方程式为_____;_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在厨房做红烧肉的时候,为了使烧出来的肉更香,向锅里面加入了少量的白酒和食醋,生成了一种具有特殊香味的物质乙酸乙酯![]() 和水,下列关于乙酸乙酯的说法正确的是
和水,下列关于乙酸乙酯的说法正确的是![]()
![]()
A. 乙酸乙酯属于有机物
B. 乙酸乙酯由4个碳原子、2个氧原子、8个氢原子构成
C. 白酒和食醋生成乙酸乙酯的反应属于化合反应
D. 乙酸乙酯中碳元素和氧元素的质量比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(12分)氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图10所示(固定装置省略)。
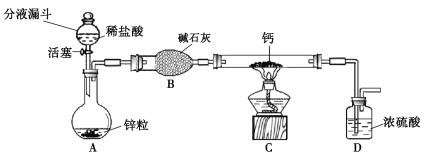
图10
回答下列问题:
(1)装置A中制取氢气的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中制取氢化钙的化学方程式为 。
(4)若不改变温度,整套装置气密性的检查方法是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图11(固定装置省略)所示连接仪器。
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化钙的纯度为 。(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示装置回答下列有关问题:
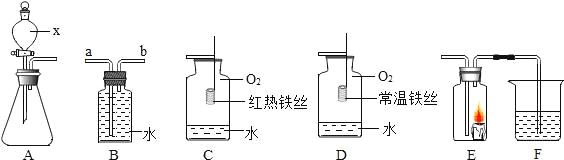
(1)仪器x的名称是_____。
(2)若用装置B收集氧气,进气口应为_____端(选填“a”或“b”)
(3)装置C中水的作用是_____。
(4)对比装置C和D,可以得出关于可燃物燃烧的条件是_____;
(5)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同。
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则E中现象说明A中产生的气体所具有的性质是_____;
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com