将锌和硫酸锌(不含结晶水)的混合物20.8 g放入179.6 g稀硫酸中,恰好完全反应,得到200 g硫酸锌不饱和溶液.求:(1)原混合物中锌单质的质量分数(2)稀硫酸中硫酸的质量分数(3)反应后所得硫酸锌溶液的质量分数.
【答案】
分析:锌和稀硫酸反应放出氢气,根据质量守恒定律,恰好完全反应前后物质质量总和之差即为反应放出氢气的质量;
根据放出氢气质量,计算参加反应硫酸的质量和反应生成硫酸锌的质量即可解决问题.
解答:解:恰好完全反应放出氢气的质量=20.8g+179.6g-200g=0.4g
设参加反应锌的质量为x,硫酸的质量为y,生成硫酸锌的质量为z
Zn+H
2SO
4=H
2↑+ZnSO
4
65 98 2 161
x y 0.4g z
65:2=x:0.4g 解之得 x=13g
98:2=y:0.4g 解之得 y=19.6g
2:161=0.4g:z 解之得 z=32.2g
原混合物中锌单质的质量分数=
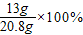
=62.5%
稀硫酸中硫酸的质量分数=
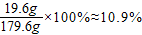
反应后所得硫酸锌溶液的质量分数=
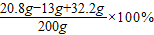
=20%
答:(1)原混合物中锌单质的质量分数62.5%;
(2)稀硫酸中硫酸的质量分数10.9%;
(3)反应后所得硫酸锌溶液的质量分数20%.
点评:反应所后得硫酸锌溶液中溶质硫酸锌的质量=原混合物中硫酸锌的质量+反应生成硫酸锌的质量.

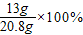 =62.5%
=62.5%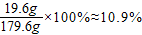
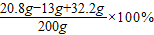 =20%
=20%
