
【题目】如图所示的四个图像,下列有关叙述正确的是( )
A.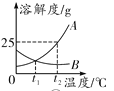 将t2 ℃的A和B饱和溶液分别降温到t1 ℃后,两溶液的溶质质量分数相同
将t2 ℃的A和B饱和溶液分别降温到t1 ℃后,两溶液的溶质质量分数相同
B. 表示高温煅烧一定质量碳酸钙的反应,纵坐标Y可表示固体中钙元素的质量分数
表示高温煅烧一定质量碳酸钙的反应,纵坐标Y可表示固体中钙元素的质量分数
C.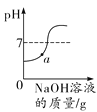 表示向稀盐酸中加入氢氧化钠溶液的反应,a点溶液中所含的溶质是HCl
表示向稀盐酸中加入氢氧化钠溶液的反应,a点溶液中所含的溶质是HCl
D.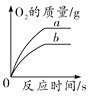 表示氯酸钾制取氧气,a是加入催化剂的反应,b表示没加催化剂的反应
表示氯酸钾制取氧气,a是加入催化剂的反应,b表示没加催化剂的反应
【答案】B
【解析】
B物质的溶解度随温度的降低而增大,应该按照t2 ℃时的溶解度进行计算,所以将A和B的饱和溶液分别降温到t1 ℃后,A的溶质质量分数为t1 ℃时A饱和溶液的溶质质量分数,B的溶质质量分数为t2 ℃时B饱和溶液的溶质质量分数,两溶液的溶质质量分数不相同,A错误;将一定质量的碳酸钙高温煅烧,加热到一定温度碳酸钙才能分解,碳酸钙高温分解生成氧化钙和二氧化碳,反应后二氧化碳逸出,钙元素质量不变,剩余固体中钙元素质量分数增大,至完全反应不再发生改变,故纵坐标Y可表示固体中钙元素的质量分数,B正确;氢氧化钠和盐酸反应生成氯化钠和水,所以向稀盐酸中加入氢氧化钠溶液的反应,a点溶液的pH<7,溶液中所含的溶质是氯化氢和氯化钠,C错误;催化剂只会影响氯酸钾分解生成氧气的速率,不会影响生成氧气的质量,D错误。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:
【题目】(2018遵义改编)盐酸、硫酸和硝酸都是重要的酸,下列是探究酸性质的实验。

(1)能区分稀盐酸和稀硫酸的是_____(选填“实验一”或“实验二”),此实验中观察到的现象是_____。
(2)如图2是装有稀硫酸的试管中加入硝酸钡溶液前后主要离子种类及个数比变化示意图。则“![]() ”代表的离子是_____(填离子符号)。
”代表的离子是_____(填离子符号)。
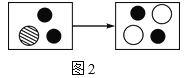
(3)实验三稀盐酸中无明显现象;稀硝酸中的现象为铜片逐渐溶解,溶液变蓝,并有气泡产生,反应为3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O,则X的化学式为_____。
(4)实验室利用氢气还原氧化铜后,试管内壁上常附着一些铜,清洗方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】梧州市某中学化学兴趣小组的同学查资料知道,乙醇(分子式为C2H6O)俗称酒精,通常情况下化学性质稳定,在一定条件下能与氧气反应。现对乙醇与氧气反应进行探究。
(探究活动一)
同学们把绕成螺旋状的红色铜丝在酒精灯的外焰上灼烧到通红,取出铜丝,发现表面变黑,趁热插入装有无水乙醇的试管中(如图),铜丝很快变为红色,并闻到刺激性气味。重复上述操作多次,得到A溶液;经称量,实验前后铜丝质量不变。

铜丝灼烧后生成的黑色物质是___,铜丝除了给反应加热外,还起到__________作用。
(提出问题) 生成的激性气味的气体是什么?
(猜想与假设)有同学提出刺激性气味的气体可能是:
猜想一:SO2猜想二:CO2。猜想三:醋酸(C2H4O2)
(讨论与结论)同学们讨论后发表看法:
小吴认为猜想一不正确,判断的依据是______________
小周认为猜想二也不正确,判断的依据是_____________
小施认为猜想三有可能正确,原因是醋酸具有挥发性,并有刺激性气味。
(探究活动二)
小施同学设计实验验证后,发现猜想三也不正确。请补充完成小施的实验操作和现象:取少量A溶液加入试管中,然后_____________
(讨论与结论)
老师提示这种刺激性气味气体来源于易挥发的B物质,其相对分子质量为44,且含有C、H、O三种元素(氢元素的质量分数不超过20%),由此可推知物质B的分子式为_____
(拓展活动)
(1)同学们再取少量A溶液加入试管中,加少量无水硫酸铜固体,变蓝色(已知:乙醇、B物质遇无水硫酸铜均不显蓝色),说明乙醇在一定条件下与氧气的反应有____生成。
(2)乙醇在微生物(醋酸菌)作用下与氧气反应能生成醋酸,写出该反应的化学方程式__________________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】葡萄的果肉和果皮中都含有丰富的营养物质。
(1)为使葡萄果实饱满、提高含糖量,在葡萄生长的中后期可适当施加硫酸钾、过磷酸钙等肥料,其中硫酸钾属于化学肥料中的_____肥。
(2)用硫酸铜配制的农药波尔多液,可以防治葡萄生长中的病害。溶解硫酸铜时不宜用铁制容器,用化学方程式表示其原因:____________________________。
(3)食用葡萄前要清洗干净,下图是一种清洗的方法。

下列说法正确的是_______(填序号)。
A.面粉有利于去除葡萄皮上的脏东西
B.清洗干净后,建议吃葡萄不吐葡萄皮
C.葡萄富含糖类物质,糖尿病人不宜多食
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高锰酸钾在生产、生活中有广泛的应用。实验小组同学查阅资料得知,草酸(H2C2O4)可使滴有硫酸的高锰酸钾溶液褪色,但不同条件下褪色时间不同,即反应的速率不同。小组同学进行了如下探究。
(提出问题)影响该反应反应速率的因素有哪些?
(作出猜想)影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
(查阅资料)硫酸锰(MnSO4)可作该反应的催化剂。
(进行实验)取A、B、C、D 4支试管,每支试管中分别加入4mL 0.08% 的KMnO4 溶液、0.4 mL 的硫酸、1mL 0.09% 的 H2C2O4 溶液。

(实验记录)
序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
A | 98% | 室温 | 无 | 72s |
B | 65% | 室温 | 无 | 129s |
C | 65% | 50℃ | 无 | 16s |
D | 65% | 室温 | MnSO4 | 112s |
(解释与结论)
(1)草酸使高锰酸钾溶液褪色反应的化学方程式如下,请在横线上补全方程式。
2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10_______+ 8H2O
(2)4支试管中作为对照实验的是_______(填序号,下同)。
(3)设计实验A和B的目的是 ______________________________。
(4)对比实验B和C可得出的结论是_____________________________。
(5)探究催化剂对该反应反应速率影响的实验是____________________________。
(反思与交流)
(6)影响该反应反应速率的因素除温度、催化剂、硫酸的浓度外,还可能有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列示意图能正确反映对应的叙述的是( )
A.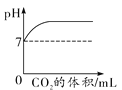 向NaOH溶液中通入一定体积的CO2气体
向NaOH溶液中通入一定体积的CO2气体
B.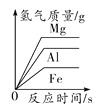 向等质量的不同金属中分别滴加足量的相同浓度的稀盐酸
向等质量的不同金属中分别滴加足量的相同浓度的稀盐酸
C.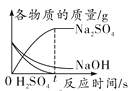 等质量、等质量分数的硫酸溶液与NaOH溶液混合
等质量、等质量分数的硫酸溶液与NaOH溶液混合
D. 两份等体积的5%的过氧化氢溶液,向其中一份中加入少量二氧化锰
两份等体积的5%的过氧化氢溶液,向其中一份中加入少量二氧化锰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是生活中的常见金属,如图所示是与铁有关的两个实验,下列说法不正确的是( )
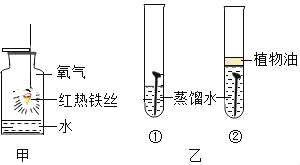
A. 实验甲中水的作用是防止瓶底炸裂
B. 实验甲中细铁丝剧烈燃烧,火星四射,生成黑色物质
C. 实验乙中试管②中植物油的作用是隔绝氧气
D. 实验乙中通过对比试管①和②的现象,说明铁生锈要有水参与
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】不同温度时![]() ,
,![]() 的溶解度如下表,图是它们的溶解度曲线。请回答下列问题:
的溶解度如下表,图是它们的溶解度曲线。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g |
| 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 13.3 | 31.6 | 63.9 | 110 | 169 | |
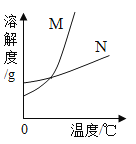
(1)图中,![]() 的溶解度曲线是_____(选填“M”或“N”).
的溶解度曲线是_____(选填“M”或“N”).
(2)20℃时,将![]() 加入100g水中,充分溶解后,溶液中氯化钠的质量分数是_____(选填序号)
加入100g水中,充分溶解后,溶液中氯化钠的质量分数是_____(选填序号)
A 40% B 28.6% C 36% D 26.5%
(3)25℃时,将![]() 、
、![]() 各30g分别加入100g水中,充分溶解后,所得溶液的溶质质量分数的关系是:
各30g分别加入100g水中,充分溶解后,所得溶液的溶质质量分数的关系是:![]() _____(选填“>”、“<”或“=”)
_____(选填“>”、“<”或“=”)![]() 。
。
(4)80℃时,分别用100g水,配制成![]() 、
、![]() 的饱和溶液,然后都降温至20℃,析出晶体的质量关系是:
的饱和溶液,然后都降温至20℃,析出晶体的质量关系是:![]() _____(选填“>”、“<”或“=”)
_____(选填“>”、“<”或“=”)![]() 。
。
(5)现用氢氧化钠固体配制100g10%的氢氧化钠溶液。需量取_____mL(水的密度为![]() )水,应选择的量筒的规格是_____mL(选填“10”、“100”或“250”)。
)水,应选择的量筒的规格是_____mL(选填“10”、“100”或“250”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学对酸、碱之间的反应进行如图所示实验。请回答下列问题。

(1)甲同学进行如图1所示实验,实验中反应的化学方程式为____________________。
(2)乙同学用氢氧化钾溶液和稀硫酸进行实验,并测得实验过程中溶液pH变化如图2所示,则通过胶头滴管加入的物质是______ ,图中曲线上C点溶液中存在的阳离子是________。
(3)虽然上述两个反应的反应物不同,但反应的实质相同,即________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com