
【题目】高锰酸钾在生产、生活中有广泛的应用。实验小组同学查阅资料得知,草酸(H2C2O4)可使滴有硫酸的高锰酸钾溶液褪色,但不同条件下褪色时间不同,即反应的速率不同。小组同学进行了如下探究。
(提出问题)影响该反应反应速率的因素有哪些?
(作出猜想)影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
(查阅资料)硫酸锰(MnSO4)可作该反应的催化剂。
(进行实验)取A、B、C、D 4支试管,每支试管中分别加入4mL 0.08% 的KMnO4 溶液、0.4 mL 的硫酸、1mL 0.09% 的 H2C2O4 溶液。

(实验记录)
序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
A | 98% | 室温 | 无 | 72s |
B | 65% | 室温 | 无 | 129s |
C | 65% | 50℃ | 无 | 16s |
D | 65% | 室温 | MnSO4 | 112s |
(解释与结论)
(1)草酸使高锰酸钾溶液褪色反应的化学方程式如下,请在横线上补全方程式。
2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10_______+ 8H2O
(2)4支试管中作为对照实验的是_______(填序号,下同)。
(3)设计实验A和B的目的是 ______________________________。
(4)对比实验B和C可得出的结论是_____________________________。
(5)探究催化剂对该反应反应速率影响的实验是____________________________。
(反思与交流)
(6)影响该反应反应速率的因素除温度、催化剂、硫酸的浓度外,还可能有_______。
【答案】CO2 B 探究硫酸溶液的浓度是否影响上述反应的速率 在硫酸溶液浓度相同、不使用催化剂的条件下,温度越高反应速率越快 B D 高锰酸钾溶液浓度、草酸溶液浓度、催化剂用量、硫酸溶液用量(合理即可)
【解析】
[解释与结论]
(1)根据质量守恒定律,反应前原子种类和数目分别是2K、2Mn、10C、16H、3S、40O,反应后原子种类和数目分别是2K、2Mn、16H、3S、20O,反应前后相差10个C原子和20个O原子,碳、氧原子个数比为1∶2,故填CO2;
(2)分析四支试管,试管A探究的是硫酸浓度对反应速率的影响,试管C是溶液温度对反应速率的影响,试管D是催化剂对反应速率的影响,只有试管B是对照实验,故填B;
(3)实验A和实验B形成对比,在其它条件相同时探究硫酸浓度是否影响反应速率,故填探究硫酸溶液的浓度是否影响上述反应的速率?;
(4)通过对比实验B和实验C,在硫酸浓度和都不使用催化剂的条件下,温度越高,反应速率越快,故填在硫酸溶液浓度相同、不使用催化剂的条件下,温度越高反应速率越快;
(5)只有D试管中加入了催化剂,所以将D试管和B试管作对比,即可得出催化剂对该反应速率的影响,故填BD;
[反思与交流]
(6)上述实验中高锰酸钾溶液的用量和浓度是固定的,草酸溶液的浓度和用量也是固定的,稀硫酸的量是固定的,改变这些定量都有可能对反应速率产生影响,此外还有催化剂的用量也有可能影响反应速率,故填高锰酸钾溶液浓度、草酸溶液浓度、催化剂用量、硫酸溶液用量(合理即可)。


科目:初中化学 来源: 题型:
【题目】下列事实与对应的解释相符合的是![]()
![]()
A. 甘蔗甜,苦瓜苦:不同分子性质不同
B. 空气能被压缩:分子体积可以变小
C. 结冰的水不能流动:结冰时水分子不再运动
D. 50mL水和50mL酒精混合后的总体积小于100mL:分子的质量和体积都很小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题。
(1)MnO2作催化剂,向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。
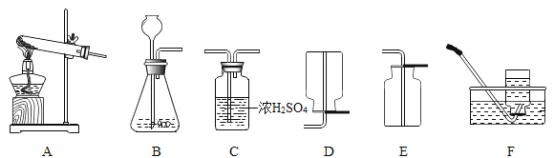
①写出用H2O2溶液制备O2的化学方程式:______。
②己知,浓硫酸常用于干燥气体。用上述反应原理制备并收集一瓶干燥的O2,从所给装置图中选择并组装一套装置,其连接顺序为______→______→______(填标号)。
(2)FeCl3溶液做催化剂,向5mL5%的H2O2溶液中加入2滴一定浓度的FeCl3溶液,立即产生大量气泡。
(已知)FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-
(问题)哪种微粒对H2O2溶液的分解起催化作用?
(假设)假设一:可能是H2O 假设二:可能是Fe3+ 假设三:可能是Cl-
(分析)①假设一不可能成立,理由是______。
(实验)
操作 | 现象 |
其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 |
其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 |
其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 |
(结论)②假设______成立,而假设和另一种假设不成立。
(3)催化剂比较
从循环利用的角度分析,______(填化学式)更适合做该反应的催化剂。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宇宙飞船上的天线是由钛镍记忆合金制造的,如图为钛元素周期表中的信息,下列所获取的信息错误的是( )

A. 钛的相对原子质量为47.87g B. 钛的元素符号为Ti
C. 钛是一种金属元素 D. 钛的核电荷数为22
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家发现用氨气(NH3)可以将NO转化成无毒物质直接排放,反应的微观示意图如下。
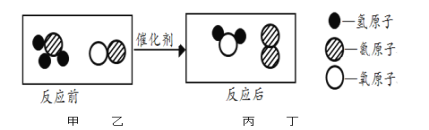
从图中获得的有关信息不正确的是
A. 甲中氮、氢原子个数比为1:3
B. 乙的相对分子质量为30
C. 反应前后分子种类不变
D. 生成物水和氮气的分子个数比为6:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线,回答下列相关问题。

(1)t1℃时,100g水中溶解20g甲,溶液刚好饱和;那么,50g水中溶解______g乙,溶液达到饱和;
(2)t2℃时,比较两物质的溶解度大小:______;
(3)t1℃时,若要将甲物质的饱和溶液变为不饱和溶液,可采用的方法是______(写出一种即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类生活生产离不开金属。
(1)国产大飞机C919大量使用合金而不用纯金属的原因是什么?______(一条即可)
(2)辽宁号航空母舰是国之重器,为保证其长期在水中航行不被腐蚀,可采取哪些措施______?(一条即可)
(3)铝由于其密度小和抗腐蚀性好的特点在高铁等交通运输方面用途广泛。
①工业上采用高温电解熔融氧化铝来制取铝,写出该反应的化学方程式______。
②铝粉和四氧化三铁粉末的混合物点燃后会生成铁和氧化铝,此反应可用于焊接钢轨,写出反应的化学方程式__________,判断反应类型为______。
(4)如图为实验室模拟工业上炼铁的原理。当观察到氧化铁处______现象时,即证明该反应已经结束可停止加热。该装置中酒精灯的目的是______。
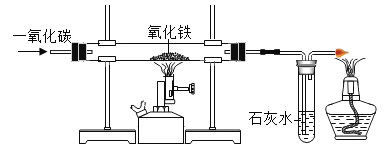
(5)若上述实验反应前后盛石灰水试管中的质量增加了1.32g,则玻璃管中有多少g氧化铁被还原_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,请用所学化学知识回答下列问题。
(1)金刚石和石墨都是由碳元素组成的单质,但是由于_______,因此它们的物理性质存在着较大的差异。
(2)用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁,其反应的化学方程式是________。
(3)铝制品形成致密的保护膜的化学方程式是_________。
(4)在电路中主要使用的是铜线,这是利用了铜的_______性。
(5)在酒厂附近常可以闻到酒味。请从微观角度加以解释________。
(6)实验室常用锌粒和稀硫酸反应制取氢气,其反应的化学方程式是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图装置完成以下实验:
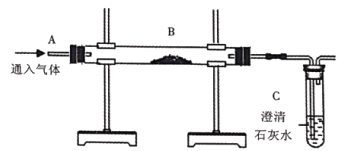
(1)探究燃烧条件:若B处盛放木炭。
I.先在A处通人氮气一段时间后 ,在B处加热 ,B、C处没有明显变化;
II.待B处冷却至室温在A处通人氧气一段时间后 ,B、C处没有明显变化;
III.在A处继续通入氧气,然后在B处加热,发现木炭燃烧 ,C处变浑浊。’
I与III对比,说明燃烧的条件之一是___________;II与III对比,说明燃烧的条件之一是___________。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用喷灯加热 ,B处可观察到的现象为___________ ,该反应的化学方程式为___________,尾气处理的方法___________。《自然》杂志刊载“绿色炼铁”技术:电解熔融的氧化铁得到铁和氧气,该反应的化学方程式:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com