
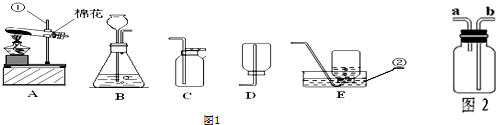
分析 (1)熟悉常用仪器的名称和用途;
(2)根据实验室应用分解过氧化氢溶液制取氧气的原理分析回答;
(3)根据实验室用高锰酸钾制取收集氧气的原理、步骤及注意的事项分析回答;
(4)据反应物状态和反应条件选择发生装置,据气体密度和溶解性选择收集装置.
解答 解:(1)由图示可知标号仪器①是铁架台,②是水槽;
(2)常温下,用分解过氧化氢溶液制取氧气,通常加入二氧化锰做催化剂,选择的发生装置是固液不需加热的B;反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)实验室用高锰酸钾制取并收集氧气时,由于是加热固体制取气体,可选用的装置组合是A;
为了防止高锰酸钾粉末进入导气管,在试管口放一团棉花;
为防止冷凝水倒流回热的试管引起试管的炸裂,试管口要向下倾斜;
用排水法收集氧气时,当气泡均匀连续时,开始收集;
用排水法收集氧气完毕后,停止加热时的操作顺序是先将导气管从水槽中移出,然后熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂.
如发生了倒吸可采取取下试管口的橡皮塞的措施来补救.
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于固体加热型,应该用A装置,若用图2装置来收集甲烷,密度小于空气,甲烷应从a端进入;
故答为:(1)①是铁架台;②是水槽;
(2)B;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)A;防止高锰酸钾粉末进入导气管;防止冷凝水倒流回热的试管引起试管的炸裂;均匀连续;熄灭酒精,而导气管没从水槽中移出;取下试管口的橡皮塞;
(4)A;a.
点评 本题比较全面考查了实验室有关的氧气的制法,要想解答好这类题目时,首先,要熟记氧气的实验室制取原理和氧气的溶解性、密度等;还要熟悉常见仪器的用途、基本的实验操作及注意事项等等.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:选择题
 实验室制取氧气的装置如图所示,下列有关叙述合理的是( )
实验室制取氧气的装置如图所示,下列有关叙述合理的是( )| A. | 锥形瓶里加入少量MnO2粉末,分液漏斗里盛放6%双氧水 | |
| B. | 锥形瓶里加入高锰酸钾固体,分液漏斗里盛放蒸馏水 | |
| C. | 该装置的优点是能控制反应的发生和停止 | |
| D. | 当发生装置中液体与固体一接触产生了气泡即刻收集 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
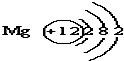 已知镁元素的原子结构示意图如图.请回答:
已知镁元素的原子结构示意图如图.请回答: 表示的意义核内有12个质子;
表示的意义核内有12个质子;查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 研究药物对抗“埃博拉”病毒 | B. | 360电脑办公软件 | ||
| C. | 我国“神舟”飞船的高能燃料 | D. | 如何解决环境污染问题 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | 氯酸钾质量 | 其它物质质量 | 待测数据 |
| ① | 1.5g | ||
| ② | 1.5g | CuO 0.5g | |
| ③ | 1.5g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com