
【题目】下图中是氧元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
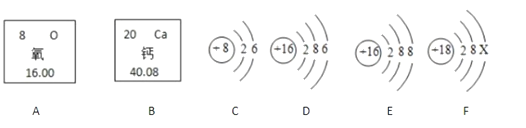
请你回答:
(1)氧元素的原子序数为_____。
(2)E粒子属于_____(填“原子”“阴离子”或“阳离子”),该粒子的符号为_____。
(3)F元素在元素周期表中的位置处于第_____周期
(4)写出由B、C、D三种元素组成的化合物的化学式____。
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“—”表示相连两种物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答下列问题:

(1)若A、B为组成元素相同的气体,E为大理石的主要成分,写出符合题意的D物质的一个化学式__。
(2)若A是能供给人类呼吸的气体,B是一种最常用的溶剂,D常用于铅蓄电池中,其浓溶液有脱水性。则D—E反应的化学方程式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】KCl与KNO3在不同温度的溶解度数据如表.则下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
A.KNO3比KCl的溶解度大
B.两物质的溶解度相等的温度在20~30℃之间
C.在20℃时,10g水中加入5g KCl可得到33.3%的KCl溶液
D.在50℃时,两物质各5g分别加入10g水中,充分溶解,均有固体剩余
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烟台有漫长的海岸线,蕴藏着丰富的海洋资源。
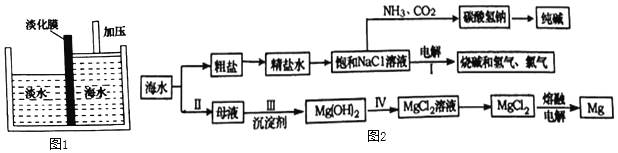
(1)海水淡化。可以采用如图1所示的膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是________(填字母序号)。
A 膜分离法的原理与滤纸过滤原理类似
B 膜分离法还可以浓缩海水中的盐类物质
C 膜分离法也是一种分离混合物的方法
D 该膜分离法的目的是除去海水中的不溶物
(2)粗盐提纯。除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42-等杂质离子,为得到较纯的氯化钠,进行如下的实验操怍①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液③加入过量的NaOH溶液;④加入适量的盐酸调节溶液的pH等于7;⑤过滤;⑥蒸发。下列操作顺序正确的是________(填字母序号),其中操作④加入适量的盐酸调节溶液的pH等于7的目的是________。
A ①③②④⑤⑥
B ③②①④⑤⑥
C ③①②⑤④⑥
D ②③①⑤④⑥
(3)海水资源综合利用的部分途径如图2。
①氨碱工业生产过程中,在加压并不断向饱和的氨盐水中通入二氧化碳的条件下,使碳酸氢钠结晶析出,该反应的化学方程式是________。
②写出步骤Ⅰ电解饱和NaCl溶液的化学方程式是________。
③海水制镁。实际生产中,步骤Ⅲ常选用________作为沉淀剂,从海水中提取MgCl2历经步骤Ⅱ、Ⅲ、Ⅳ三步转换的主要目的是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酒精是一种无色、透明、有特殊气味的液体,易挥发,能与水以任意比互溶,常用作酒精灯和内燃机的燃料,是一种绿色能源,当点燃酒精灯时,酒精在灯芯上气化后燃烧生成水和二氧化碳。
(1)根据以上叙述,可归纳出酒精的物理性质是____;化学性质是____;酒精的用途是___。
(2) 实验中,不小心将酒精灯碰倒在桌上燃烧起来,合理简单的灭火措施是_______。
(3)下列仪器不能用酒精灯加热的是(______)
A燃烧匙 B试管 C量筒 D蒸发皿
(4)某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。

① 写出铁丝在氧气中燃烧的化学符号表达式: ___________________________________。
② 探究一:蜡烛燃烧产生火焰的原因是什么? 点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由____________(填“固态”或“气态”)物质燃烧形成的。
③ 探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其____________(填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰________。由此推测:钠在燃烧时,________(填“有”或“没有”)火焰产生。
④ 根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点______硫燃烧时的温度(填“>”或“<”或“=”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,反应④常用于检验二氧化碳,E是一种金属氧化物,能与A反应。它们之间的转换关系如图所示:
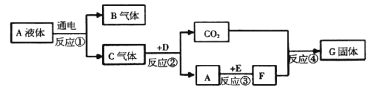
(1)写出下列物质的化学式:A_________、E_________。
(2)写出以下反应的化学方程式:
反应②______。
反应④______。
(3)E在日常生活中用途广泛,请写出其中一点_____。
(4)B与其它燃料相比其优点有________等(写一个即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】气在生产、生活中有广泛用途,研究其制取、性质和用途十分重要.
(1)工业上用氮气和氢气在高温高压和催化剂存在时合成氨;实验室用氯化铵和熟石灰在加热条件下制取氨气,同时生成氯化钙和水.请分别写出有关反应的化学方程式___________.实验室制取氨气的发生装置与制取哪种气体的相似,请写出实验室制取该气体的化学方程式:__________
(2)如图是氨气性质的趣味实验:圆底烧瓶中充满氨气,当挤压胶头滴管并打开止水夹时,烧杯中的水迅速进入烧瓶,形成美丽的“喷泉”,进入烧瓶的水变成红色.由该实验可得出哪些结论___________
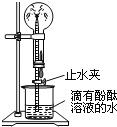
(3)氨气常作制冷剂及化肥,同时,它还可作清洁能源.已知表信息:
性质 | 颜色、气味 | 沸点(℃) | 25℃水中溶解度(g/L-1) |
NH3 | 无色、刺激性 | -33 | 456 |
H2 | 无色、无味 | -253 | 0.0015 |
一定条件下氨气在纯氧中完全燃烧生成水和氮气,写出该反应的化学方程式______________________.
液氨有望和液氢一样成为新一代绿色能源.与H2相比,用NH3作燃料的优点之一是便于储存和运输;优点之二是泄漏时易发现且便于处理.请对氨气的优点加以解释说明_________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图回答问题:
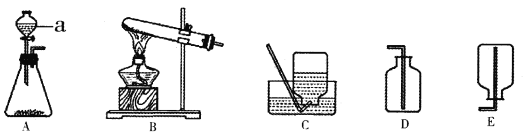
(1)写出仪器a的名称,a是___________________。
(2)若用A装置制取氧气,反应的文字表达式是___________,该方法与高锰酸钾制氧气相比具有的优点是________________。(写一条即可)
(3)实验室收集O2和CO2 都能用的收集装置是___________。(填字母编号,下同),检验CO2是否收集满的方法是:_______________。
(4)实验室也可加热氯酸钾和二氧化锰的固体混合物来制取氧气,在此反应中,二氧化锰起_________作用,发生装置应选_____________。
(5)某同学用浓盐酸和大理石在图甲装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红。已知:浓盐酸具有挥发性,挥发出的氯化氢气体溶于水显酸性。对石蕊变红这一变化的合理解释是_____________ (填序号)
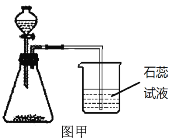
A 产生的CO2直接使石蕊试液变红
B 挥发出的氯化氢溶于水使石蕊试液变红
C 产生的CO2与水反应生成H2CO3使石蕊试液变红
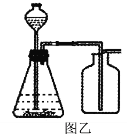
(6)若某同学用图乙装置制取了一瓶无色、无味的气体(纯净物),你推测该气体可能是____________,使用最简便的方法证实你的推测:(写出现象和结论)_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料广泛应用于生产、生活中。
①下列用品中,主要利用金属导热性的是_______(填字母)。
A 金饰品 B 铁锅 C 铜导线
②铝在空气中与氧气反应,其表面会生成一层致密的氧化物薄膜,从而阻止铝进一步被氧化。该反应的化学方程式为_______。
③向含有氯化铜、氯化亚铁和稀盐酸的混合溶液中加入过量镁粉,充分反应后过滤,滤液中含有的溶质是_______(写化学式)。
④铁制容器不能用来盛放农药波尔多液(波尔多液的主要成分是硫酸铜和氢氧化钙),用化学方程式表示其原因_______。
⑤某钢铁厂每天需消耗3500t含![]() 80%的赤铁矿石,该厂理论上可日产含
80%的赤铁矿石,该厂理论上可日产含![]() 98%的生铁的质量是_______t。
98%的生铁的质量是_______t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com