
【题目】现有氧化铜和铜的混合物,对其成分进行分析.取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:(反应的化学方程式:CuO+H2SO4=CuSO4+H2O)
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体质量/g | 8 | 6 | 4 | 3 | m |
试回答下列问题:
(1)上述表格中m的值为______,10g样品中CuO的质量为______g.
(2)计算所加入稀硫酸中溶质的质量分数?______
(3)计算第三次加稀硫酸反应后所得溶液中溶质的质量分数?(精确到0.1%)_____
【答案】3 7 12.25% 18.2%
【解析】
(1)根据实验数据分析出加入的稀硫酸与参加反应的氧化铜的质量比关系,进而可确定m的值;固体前后减少的质量为氧化铜的质量;
(2)根据实验数据可知20克稀硫酸与2克氧化铜恰好完全反应,利用氧化铜与硫酸反应的化学方程式,根据2克氧化铜的质量求出20克稀硫酸中溶质的质量,最后根据![]() ,求出稀硫酸中溶质的质量分数;
,求出稀硫酸中溶质的质量分数;
(3)第三次反应后60克稀硫酸与6克氧化铜恰好完全反应,所得溶液中溶质的质量分数=![]() ,溶质为硫酸铜,根据6克氧化铜的质量可求出,所得溶液的质量=参加反应的氧化铜的质量+所加稀硫酸的质量。
,溶质为硫酸铜,根据6克氧化铜的质量可求出,所得溶液的质量=参加反应的氧化铜的质量+所加稀硫酸的质量。
(1)根据实验数据分析可知,第一次加入20克稀硫酸,有10g-8g=2g CuO被消耗掉,因此每20克稀硫酸与2克氧化铜恰好完全反应,第四次加入20克稀硫酸后只减小了1克氧化铜,说明氧化铜已反应完,第五次再加入稀硫酸,剩余固体的质量也不会减少,所以m的值为3;氧化铜的质量=10g-3g=7g;
(2)设20克稀硫酸中溶质的质量为x
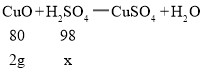
![]()
x=2.45g
H2SO4溶液中溶质质量分数=![]() ×100%=12.25%;
×100%=12.25%;
(3)设第三次加稀硫酸反应后所得溶液中溶质的质量为y,
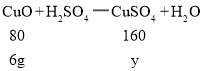
![]()
y=12g
第三次加稀硫酸反应后所得溶液中溶质质量分数=![]() ×100%≈18.2%。
×100%≈18.2%。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:初中化学 来源: 题型:
【题目】高速铁路作为一种安全可靠、运载量大、低碳环保的运输方式,已经成为世界铁路发展的重要趋势,根据图示回答下列问题:
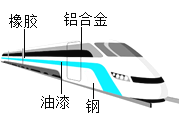
(1)图中标示的高速列车材料中,属于金属材料的是________(任写一种);
(2)高速列车使用的金属材料大多是合金而不是纯金属,这是因为合金具有更多优良性能。例如,铝合金比纯铝的硬度_______(填“大”或“小”),不锈钢锅比纯铁的抗腐蚀性_______(填“强”或“弱”)。
(3)高速列车表面喷漆除美观外,主要是为了_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学为了研究(Cu﹣Zn合金)样品中铜的含量,取该样品20g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如下图所示.请计算:
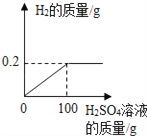
(1)反应的硫酸质量为多少g。
(2)求样品中铜的含量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁、铝、锌、铁与稀盐酸或稀硫酸之间的反应规律及图象正确的是( )
|
|
|
|
A等质量的镁、铝、锌、铁与足量酸反应,氢气质量与反应时间的关系图象 | B等质量的镁、铝、锌、铁与足量酸反应,氢气质量与酸溶液的关系图象 | C等量酸与足量镁、铝、锌、铁反应,氢气质量与反应时间的关系图象 | D等量酸与足量镁、铝、锌、铁反应,氢气质量与金属质量的关系图象 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
纯净物 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
A.反应后X的质量为1.5g B.X中一定含有碳元素和氧元素
C.X中一定含有碳元素和氢元素 D.X中两种元素的质量比是1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体的溶解度曲线。
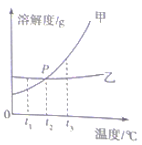
(1)P点的含义是_____。
(2)若甲物质中混有少量乙物质,要提纯甲物质,可采用的方法是_____。
(3)t3℃时将等质量的甲、乙饱和溶液降温至t1℃(其他条件不变),所得溶液中溶剂的质量关系为:甲_____ (填“>”“<”或“=”)乙。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐在我们的生活中有着重要的作用。
(1)硫酸是一种常见的酸,下列物质不能与稀硫酸发生复分解反应的是_____(填字母)。
A NaOH溶液 B NaCl溶液 C K2CO3溶液 D Ba(NO3)2溶液
(2)氢氧化钠是一种常见的碱,聪聪同学为了探究实验室中久置的氢氧化钠固体的成分,进行了如图所示的实验。
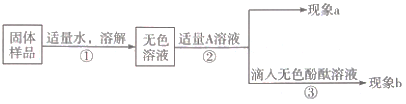
①若现象a为有气泡产生,则说明氢氧化钠已经变质,请写出产生气泡的化学方程式:_____。
②若A是Ca(OH)2溶液,现象a为有白色沉淀产生,现象b为酚酞溶液变红,该实验_____(填“能”或“不能”)说明氢氧化钠为部分变质,原因是什么_____?
(3)氯化钠是一种常见的盐,以海水为原料得到精盐NaCl和提取镁的工艺流程如图(此题中微溶物视为可溶物,所加试剂均过量)。
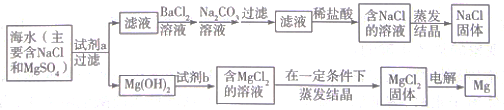
①Mg(OH)2与试剂b反应的化学方程式为_____。
②试剂a不可能是下列物质中的_____(填字母)。
A KOH溶液 B NaOH溶液 C Ca(OH)2溶液 D Ba(OH)2溶液
③在蒸发结晶的过程中,玻璃棒的作用是_____。
(4)纯碱和小苏打都是生活中常见的盐,二者性质上有一区别是小苏打受热易分解产生纯碱、二氧化碳和水,而纯碱不易分解。将25g小苏打和纯碱的固体混合物装入试管中,加热至反应完全后,可以得到18.8g固体物质。请计算原固体混合物中小苏打的质量_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学中常见的五种无色气体,其中两种是单质,另三种是化合物,E是一种化石燃料,X在常温下是液体。它们之间有下图所示的转化关系(图中未注明反应条件。)
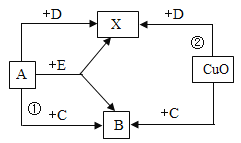
(1)写出指定物质的化学式:
A______ D______ E______
(2)写出反应①的化学反应方程式_______,该反应从能量的变化来看,属于____反应(填“放热”或“吸热”)。
(3)写出反应②的化学反应方程式_______,该实验中先通入D气体,再加热的原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学学习小组在学习常见的盐的性质后,完成了如下实验。该学习小组对废液杯上层清液的溶质的成分进行了探究。请完成以下探究过程,并将答案填入空白相应位置。
(提出问题)上层清液中含有什么溶质?
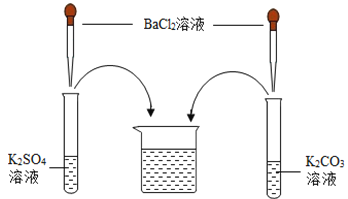
(作出猜想)Ⅰ溶质仅为_____(填化学式);Ⅱ溶质为KCl和BaCl2;Ⅲ溶质为KCl和_____(填化学式);Ⅳ溶质为KCl和K2CO3;Ⅴ溶质为KCl、K2SO4和K2CO3;Ⅵ溶质为KCl、K2SO4、BaCl2和K2CO3。
(交流讨论)小强同学认为猜想Ⅵ一定是错误的,他的理由是_____。
(设计方案)
实验操作 | 现象 | 结论 | |
取少量废液缸中上层清液,分装于甲、乙两支试管中 | 先向甲试管中滴加盐酸至过量 | 无明显现象 | 猜想Ⅳ、Ⅴ不正确 |
再向乙试管中滴加_____溶液(填化学式) | _____ | 猜想Ⅱ正确 | |
(交流反思)学习小组经过讨论认为:实验过程中无须使用AgNO3溶液,其理由是_____(用文字表述)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com