
【题目】某兴趣小组利用如图装罝(省略夹持仪器)探究二氧化碳与氢氧化钠溶液的反应

(实验步骤)
①将足量的氢氧化钠浓溶液装入分液漏斗中。
②打开止水夹K1,待氢氧化钠浓溶液完全进入广口瓶之后立即关闭K2。
③待充分反应后,打开止水夹K2
(实验现象)
整个实验过程中,观察到注射器中的液体_____。U型管中_____,广口瓶中的液体出现浑浊。
(实验解释)
步骤②中发生反应的化学方程式为_____。产生上述现象的原因_____。
【答案】液体自动喷出或自动喷入U型管或进入U型管 液体变红,并有部分液体沿导管进入广口瓶(有液体进入即给分) CO2+2NaOH=Na2CO3+H2O 二氧化碳与氢氧化钠反应生成碳酸钠,广口瓶中气压变小,流入瓶中的氢氧化钙与碳酸钠反应产生碳酸钙白色沉淀,此时U型管右侧气压也变小,使注射器中液体自动喷出,酚酞溶液遇碱性氢氧化钙溶液变为红色
【解析】
实验现象:
氢氧化钠浓溶液和二氧化碳反应生成碳酸钠和水,化学方程式为:![]() ;气体被消耗,瓶内压强减小,U型管左侧的液体有部分液体沿导管进入广口瓶;由于U型管左侧的液体有部分液体沿导管进入广口瓶,导致U型管中右侧空气中压强减小,从而大气压将压注射器,造成注射器中的液体自动喷出,碱溶液能使无色酚酞变红;广口瓶中出现浑浊现象的原因二氧化碳与氢氧化钠反应生成的碳酸钠与氢氧化钙反应产生碳酸钙白色沉淀;
;气体被消耗,瓶内压强减小,U型管左侧的液体有部分液体沿导管进入广口瓶;由于U型管左侧的液体有部分液体沿导管进入广口瓶,导致U型管中右侧空气中压强减小,从而大气压将压注射器,造成注射器中的液体自动喷出,碱溶液能使无色酚酞变红;广口瓶中出现浑浊现象的原因二氧化碳与氢氧化钠反应生成的碳酸钠与氢氧化钙反应产生碳酸钙白色沉淀;
故整个实验过程中,观察到注射器中的液体液体自动喷出或自动喷入U型管或进入U型管;U型管中液体变红,并有部分液体沿导管进入广口瓶,广口瓶中的液体出现浑浊。
实验解释:
步骤②中,氢氧化钠浓溶液和二氧化碳反应生成碳酸钠和水,化学方程式为:![]() 。
。
产生上述现象的原因是:二氧化碳与氢氧化钠反应生成碳酸钠,广口瓶中气压变小,流入瓶中的氢氧化钙与碳酸钠反应产生碳酸钙白色沉淀,此时U型管右侧气压也变小,使注射器中液体自动喷出,酚酞溶液遇碱性氢氧化钙溶液变为红色。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】通过学习了酸的通性,我们可以对硫酸的化学性质进行验证和总结,下图所示“—”表示物质两两之间能发生化学反应。请根据下图,回答问题。

(1)浓硫酸能使纸张变黑是因为它有_____性,在稀释浓硫酸时要将_____,并不断搅拌。
(2)紫色石蕊试液遇硫酸呈_____色。
(3)补充一个实验,完善硫酸的化学性质,X可以是_____(用化学式表示),它的物质类别是_____(填“单质”、“氧化物”、“酸”、“碱”或“盐”)。
(4)请写出氢氧化铁与硫酸反应的化学方程式_____,该反应的现象是_____。
(5)为测定某硫酸中溶质的质量分数,甲同学取该硫酸样品50g,向其中加入过量锌粒,充分反应后收集到0.4克氢气,请完成下列计算与
Ⅰ.收集到的氢气是:_____mol;
Ⅱ.该硫酸中溶质的质量分数。_____(根据化学方程式计算)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学在实验室发现一瓶敞口放置的过氧化钠(Na2O2)固体,他们对该固体是否变质产生了兴趣,对固体成分进行了实验探究。
(查阅资料)
①在标准状况下,氧气的密度是1.429g/L.在室温下,1L水中能溶解约30mL的氧气。
②过氧化钠能与二氧化碳反应:2Na2O2+2CO2═2Na2CO3+O2↑
③过氧化钠能与水反应:2Na2O2+2H2O═4NaOH+O2↑
④BaCl2溶液呈中性。
(成分猜想)固体中可能有Na2O2、NaOH和Na2CO3中的一种或几种。
(实验验证)
实验步骤 | 实验现象 | 结论或化学方程式 |
(1)取少量样品于试管中,加水溶解,并立即将带火星的木条伸入试管中。 | 有气泡产生,_______ | 证明固体中含有Na2O2 |
取步骤(1)所得溶液于试管中,滴加过量的BaCl2溶液 | 有白色沉淀生成 | 证明固体中含有Na2CO3,化学方程式为_______ |
取步骤(2)中的上层清液于试管中,滴入1~2滴酚酞试液 | 溶液变红 | 证明固体中含有NaOH. |
(分析交流)经过讨论分析,同学们认为步骤(3)中的结论不合理,不能证明固体中含有NaOH,理由是_______。
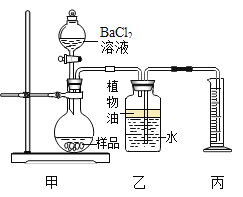
(继续探究)为确定固体中是否含有NaOH,取一定质量的样品,利用如图装置进行实验验证。(BaCl2溶液的体积和温度变化对气体体积的影响忽略不计)
(1)装置乙中植物油的作用是_______。
(2)待反应完全后,根据收集所得气体的体积,进行相关计算,得出样品中_______的质量。
(3)再将烧瓶中的沉淀进行过滤、洗涤、烘干、称量,进行相关计算,得出样品中_______的质量。
(实验结论)经过实验数据分析,得出固体中不但含有Na2O2和Na2CO3,还含有NaOH.证明含有NaOH的依据是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类文明的发展和社会的进步同金属材料关系十分密切。
(1)我国“蛟龙”号载人潜入器上使用了钛合金,钛合金放在海水中数年仍光亮如初,这是因为它_____。(填字母代号)
a.易加工 b.密度小 c.熔点高 d.耐腐蚀
(2)铁制品在潮湿的空气中容易生锈,用盐酸清除铁锈的化学方程式为_____。
(3)向含有 Cu(NO3)2 和AgNO3 的混合溶液中加入一定量的锌粉,充分反应后过滤,所得固体的质量等于加入锌粉的质量。
①请分析所得固体的成分_____。
②写出一个有关反应的化学方程式_____。
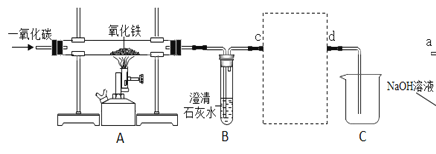
(4)钢铁是基本的结构材料,称为“工业的骨骼”。实验室可利用下图装置模拟炼铁反应。
 a
a![]() b
b
①写出 A 装置玻璃管内发生反应的化学方程式_____。
②虚线框内选择 D 装置用于吸收 CO2 并收集 CO,装置的连接顺序是:c 接_____,_____接 d。
③请设计实验证明 C 装置烧杯中溶质的成分。_____(简要写出实验步骤、现象及结论)
(5)国产 C919 大型客机上使用了大量的铝合金。工业上常用电解熔融的氧化铝冶炼铝,同时得到氧气。计算电解 20.4 t 氧化铝,理论上能生成铝的质量是多少_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
(1)用小木棍蘸取少量浓硫酸,放置一会后,可观察到 ______ .
(2)用温度计的液泡蘸取少量浓硫酸,放置在空气中一会儿,可观察到温度计显示温度升高,其原因是 ______ .
(3)如果不慎将浓硫酸沾到皮肤上,应立即 ______ ,然后______ .
(4)实验室用98%的浓硫酸(密度1.84g/cm3)配制100g溶质质量分数为20%的稀硫酸.浓硫酸稀释过程如图所示,b中盛放的物质是 ______ ,a的作用是 ______ .
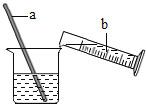
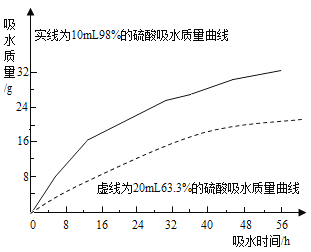
(5)探究浓硫酸的吸水性.兴趣小组把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,称量、观察、记录、分析.根据室温环境下实验的数据绘成的曲线如图:
①稀释浓硫酸时,应将 ______ 缓缓地注入盛有 ______ 的烧杯中并不断搅拌;
②由如图曲线你能得到的实验结论有哪些?(写两点) ______ 、 ______ .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C、G都是金属单质,I为无色气体.它们的相互转化关系如图所示:
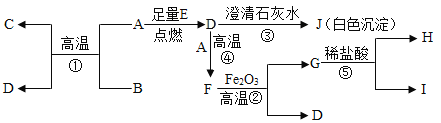
请回答:
(1)写出下列物质的化学式:A_____。
(2)反应①②③④⑤中属于置换反应的为_____(填序号)。
(3)写出反应②的化学方程式_____,其中_____为该反应的氧化剂。
(4)写出反应⑤的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为常见的实验装置,根据下列要求回答问题(装置可重复使用)。
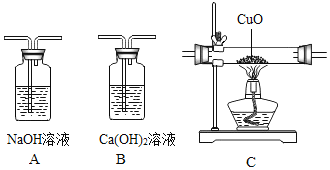
(1)将含有水蒸气的一氧化碳气体干燥后还原氧化铜,则该气体先要通过装有_____(填药品名称)的洗气瓶进行干燥再通入C装置。写出C装置中一氧化碳还原氧化铜的化学方程式_____,当黑色的CuO全部变成亮红色物质后,应先进行的实验操作是_____(填“熄灭酒精灯”或“停止通CO”)。
(2)如果要检验某混合气体中是否含有CO2和CO,则仪器的连接顺序是_____→_____→_____→_____→_____→尾气处理装置,请写出一个具体的尾气处理装置_____。C装置中酒精燃烧的化学方程式为_____。
(3)如果要验证某氢气和二氧化碳的混合气体中是否含有CO,仪器的连接顺序是A→B→C→B→尾气处理装置。则第一个B装置中的作用是_____,写出第二个B装置中发生反应的化学方程式_____。如果没有A装置,对实验有何影响_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无处不在的溶液。溶液对于自然界中的生命活动和人类生产活动具有重要意义。
(1)医院输液常用的0.9%的生理盐水来稀释其他药物。
①生理盐水中的溶质和溶剂分别是__________(写化学式),小组同学采用以下方法来测定某品牌生理盐水中溶质的质量分数,请将实验方案填写完整。
物理方法:取ag生理盐水,_________,根据实验数据计算。
化学方法:取ag生理盐水,______________,根据实验数据计算。该方法中发生化学反应的方程式为___________。
②盐酸左氧氟沙星是常用抗菌药物,每瓶含盐酸左氧氟沙星固体0.4g,使用时用0.9%的生理盐水配成注射液,其注射液中盐酸左氧氟沙星的溶质质量分数不超过10%,则使用时每瓶至少需加入生理盐水(密度约为1g/mL)___________mL.
(2)实验表明,氯化钠、氯化钙等物质溶于水后会使水的凝固点降低,可用作融雪剂。由此可见,混合(或熔合)可以改变物质的性质,从而使物质更好的被人类利用。试从所学的知识中再举一例说明上述观点_________________。
(3)溶解性是物质重要的物理性质,溶解度可以定量表示物质的溶解性,甲、乙两种固体的溶解度曲线如图2所示,某同学将甲、乙固体各30g分别加入100g水中后,进行了如图1所示的实验:
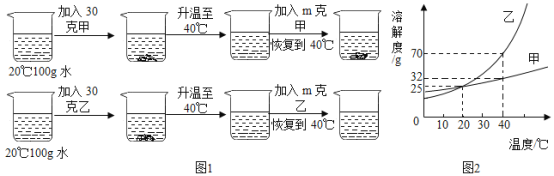
①10℃时,甲乙两种物质的溶解度大小关系:甲_____乙(填“<”、“>”或”=”)若甲中溶有少量乙,可采用_________的方法提纯甲。
②m的取值范围__________
(4)溶液中的化学反应
①土壤中含有水分,里面溶解了多种物质(包括化肥),形成植物赖以生长的土壤溶液,经测定某海边土样中的可溶性物质中含氯化钠、氯化钙和碳酸钠等,农民在该地块中施加氯化铵效果不明显,原因可能是__________.
②小东同学向盛有硝酸锌和硝酸银混合液的烧杯中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,观察到有气泡产生。根据观察到的现象,请你对滤液中溶质的成分做出推理_______________。
③氢化钙(CaH2)是白色细颗粒状固体,常用作登山运动员的能源提供剂,能与水发生如下反应并放出大量的热:![]() 。将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,滤液成分可能是(有几种可能写几种)__________________。
。将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,滤液成分可能是(有几种可能写几种)__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl2溶液呈中性)。求:
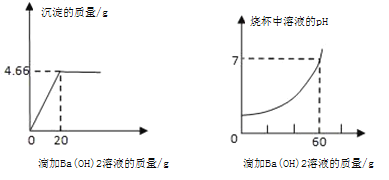
(1)完全反应后生成沉淀的质量为_____g;
(2)氢氧化钡溶液的质量分数为_____;
(3)计算20g混合溶液中HCl的质量为多少?_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com