
| A. | 大多数分子是由原子构成的 | B. | 原子都是由质子、中子、电子构成的 | ||
| C. | 只有原子得失电子才可形成离子 | D. | 分子、原子、离子都可构成物质 |
科目:初中化学 来源: 题型:选择题
| A. | Y>X>Z | B. | Y>Z>X | C. | X>Y>Z | D. | X>Z>Y |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 盐酸溶液 浓度 | 反应开始时酸溶液的 温度 | 反应开始到2分钟产生的 气体体积 | 反应结束共产生 气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 102mL | 175mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于置换反应 | |
| B. | 铝发生了还原反应 | |
| C. | 可用于工业生产,说明锰的市场价值高于铝 | |
| D. | 反应前后,锰元素的化合价降低 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
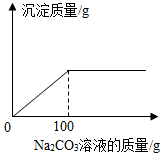 某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克水使其完全溶解,然后向其中加入10.6%的Na2CO3溶液,生成沉淀的质量与加入Na2CO3溶液的质量关系如图所示(恰好完全反应时所得食盐溶液仍为不饱和溶液).
某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克水使其完全溶解,然后向其中加入10.6%的Na2CO3溶液,生成沉淀的质量与加入Na2CO3溶液的质量关系如图所示(恰好完全反应时所得食盐溶液仍为不饱和溶液). 查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含有氧元素的物质叫氧化物 | |
| B. | 由一种元素组成的物质是一定单质 | |
| C. | CO2通入紫色石蕊溶液中溶液变红,是因为CO2显酸性 | |
| D. | 酸类物质具有相似化学性质的原因是因为它们溶液中都含有H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com